La sclerosi multipla (Sm) colpisce, in genere, donne e uomini di età tra i 20 e i 30 anni, ovvero proprio nella fascia di età in cui si delinea il progetto di vita e si fanno scelte cruciali per il futuro (Scalfari et al., 2010; Ghezzi, Zaffaroni, 2007). La malattia colpisce il fisico in maniera complessa e multiforme, incidendo fortemente sulla sfera sociale della persona che ne è affetta, ma anche su quella dei familiari.
I segni e i sintomi d’esordio dipendono dalla localizzazione delle lesioni a livello cerebrale e possono essere molto variabili da soggetto a soggetto. Lo stesso vale per la frequenza con cui essi compaiono (Figura 1): alcuni sintomi sono decisamente frequenti, altri sono rari o compaiono solo dopo anni dalla diagnosi (Noseworthy et al., 2000).
Figura 1 – Frequenza dei sintomi più comuni all’esordio
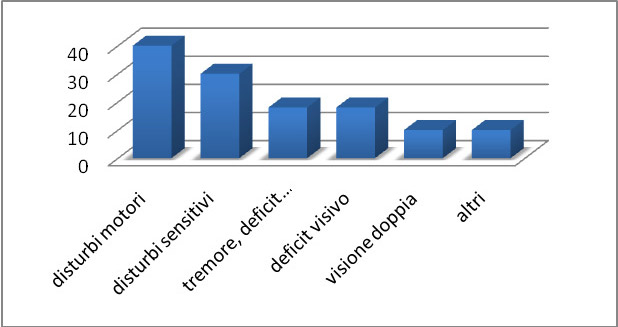
Non essendo stata riconosciuta un’unica causa per la Sm, il trattamento non agisce sull’eziologia, piuttosto sui meccanismi con cui la malattia si sviluppa (Scalfari et al., 2010). Durante il decorso della malattia, secondo l’andamento (remissione e/o riacutizzazione), della risposta e della tolleranza al farmaco, il trattamento è adattato utilizzando farmaci definiti di prima, seconda, terza linea, fino alla quarta con l’uso delle cellule staminali.
Questi nuovi trattamenti farmacologici sembrano portare dei risultati positivi: rallentano la progressione e l’evoluzione della malattia, garantendo una qualità di vita accettabile alle persone che ne sono affette.
La nostra esperienza
Per valutare la qualità della vita dei nostri pazienti, abbiamo preso in considerazione il trattamento con Natalizumab, un anticorpo monoclonale oggi approvato per le forme di Sm recidivante-remittente (Rr). Si tratta di un farmaco di seconda linea che interferisce con il passaggio delle cellule immunitarie attraverso la barriera ematoencefalica, impedendo quindi alle stesse di raggiungere e aggredire la mielina (Bielekova, Becker 2010; Stuve et al., 2008). La somministrazione per via endovenosa è eseguita una volta al mese.
Abbiamo voluto valutare la percezione della qualità della vita dei nostri pazienti in trattamento con questo preparato, somministrando un questionario anonimo costituito da 25 domande chiuse a risposta multipla. Lo strumento d’indagine prendeva in considerazione le attività di vita quotidiana, l’attività lavorativa, la salute fisica e lo stato emotivo, la sfera sociale e il dolore. Per estrapolare le domande per noi più significative abbiamo utilizzato come riferimento la versione breve del questionario Sf-36 (12/94 IQOLA SF-36 Italian Version 1.6).
I questionari sono stati illustrati e somministrati a tutti i 26 pazienti, in trattamento con Natalizumab: nessun paziente ha avuto bisogno di supporto nella compilazione.
La maggior parte delle persone che nel nostro centro sono sottoposte a questo specifico trattamento ha un’età compresa tra i 31 e i 45 anni (18 persone su 26) e sono per lo più donne (16 persone su 26). Per 21 persone la diagnosi risale a più di tre anni fa.
Al momento dell’indagine 18 pazienti lavoravano o studiavano.
I sintomi più frequenti nel tempo e lamentati dalla maggior parte dei pazienti sono: la debolezza e la fatica fisica (13 soggetti sul totale), il formicolio agli arti, le parestesie e la mancanza di equilibrio (12 soggetti sul totale).
Solo 3 pazienti hanno manifestato gli effetti indesiderati descritti per il farmaco: affaticamento, dolori articolari e cefalea. Dall’analisi dei questionari compilati emerge che 19 persone considerano buono il proprio stato di salute, 14 invece riferiscono un deciso miglioramento dopo l’inizio del trattamento con Natalizumab.
Attività fisiche impegnative come correre, camminare, sollevare oggetti pesanti, attività che richiedono un impegno fisico moderato come spostare il tavolo, attività domestiche, non comportano alcuna difficoltà per la maggior parte delle persone. Anche attività come salire le scale, fare il bagno, vestirsi, fare acquisti, prendere l’autobus, inginocchiarsi e piegarsi sono svolte in completa autonomia o con pochissime difficoltà quasi da tutti.
A lamentare problemi nelle attività fisiche sono le persone in trattamento da più di un anno e con diagnosi superiore ai tre anni: 9 dei nostri pazienti hanno dovuto limitare in modo importante il tempo dedicato al lavoro e allo studio, mentre sette hanno riferito difficoltà nello svolgere le normali attività di lavoro.
Per la maggior parte delle persone (19) la malattia non è causa di difficoltà nella concentrazione; lo è, invece, per 7 soggetti. Nonostante la consapevolezza dell’evoluzione della malattia, il tono dell’umore è stato considerato buono da 13 pazienti. La stanchezza fisica è stata riferita da 24 persone: per alcune è stata occasionale, per altri, invece, più frequente (Figura 2).
Le aspettative dei pazienti nei confronti dei trattamenti sono risultate diversificate: alcuni si attendono un miglioramento almeno lieve, altri una stabilizzazione della malattia o un miglioramento significativo.
Figura 2 – La presenza del sintomo stanchezza
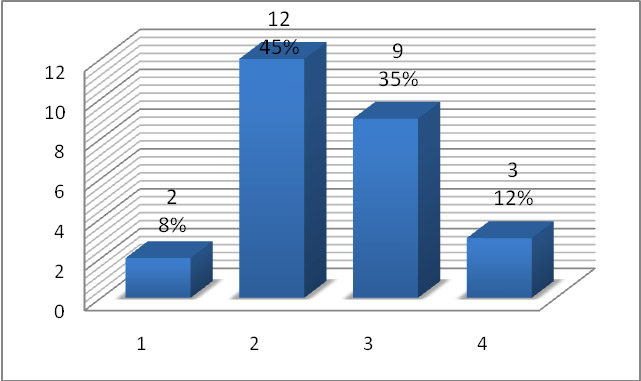
I pazienti che hanno risposto al questionario si collocano, per la maggior parte, tra il livello 1 e 4,5 della scala Edss (Expanded disability status scale), strumento che valuta le disabilità neurologiche. Sono infatti deambulanti e hanno deficit di grado lieve o moderato, non interferenti sull’autonomia o con minime limitazioni nell’attività completa quotidiana. Solo alcuni sono tra il livello 5 e 6 della scala: non sono completamente autonomi, hanno modeste limitazioni nelle attività di vita quotidiana e necessitano di assistenza saltuaria e costante.
I risultati che abbiamo ottenuto evidenziano la necessità di dotarci di uno strumento operativo per la documentazione dei problemi a carattere assistenziale dei pazienti in trattamento con Natalizumab nonché di una pianificazione assistenziale che favorisca l’integrazione tra professionisti.






