IMPLICAZIONI PER LA PRATICA
– L’infermiere appositamente formato è in grado di eseguire l’espianto di loop recorder in sicurezza;
– Nell’esperienza del nostro centro, l’affidamento agli infermieri dell’espianto di loop recorder ha migliorato anche l’allocazione delle risorse.
INTRODUZIONE
I loop recorder impiantabili (implantable loop recorder – ILR), conosciuti anche come monitor cardiaci iniettabili (injectable cardiac monitor – ICM) nella loro evoluzione miniaturizzata più recente, sono sistemi di monitoraggio sottocutanei utilizzati per la diagnosi di patologie del ritmo cardiaco per cui è necessario un monitoraggio continuo e a lungo termine.
Al loro ingresso sul mercato, avvenuto circa 20 anni fa, gli ILR erano utilizzati principalmente nel percorso diagnostico dei pazienti con sincope di dubbia origine o per stabilire la correlazione tra sintomatologia del paziente e aritmie, quali tachicardie ventricolari, bradicardia o pause. Successivamente, con l’introduzione nel dispositivo di appositi algoritmi per il rilevamento della fibrillazione atriale, l’ILR ha assunto un ruolo sempre più importante nella diagnosi e nel monitoraggio dell’esito del trattamento di questa aritmia, asintomatica in molti casi, sia nella popolazione sottoposta all’ablazione delle vene polmonari sia in quella con ictus criptogenico (Moya, 2009; Kirchhof, 2016). La miniaturizzazione degli ICM, rispetto ai precedenti ILR, e la creazione di strumenti appositamente sviluppati per renderne l’impianto minimamente invasivo (Todd, 2014; Pürerfellner, 2015) hanno portato alcune unità di cardiologia ad affidare agli infermieri attività tradizionalmente svolte dal medico elettrofisiologo, quali la fase di impianto e di programmazione dell’ICM, la fase di educazione del paziente all’utilizzo del dispositivo e del controllo remoto e la fase di revisione dei dati trasmessi e di contatto con il paziente nella fase di follow-up remoto (Roebuck, 2015). L’implementazione di protocolli gestionali che delegano il primo impianto e il follow-up del paziente con ICM agli Infermieri appositamente formati si è mostrato sicuro e ha apportato benefici sia al paziente sia alla struttura sanitaria (Cervellione, 2018; Lim, 2019, Eftekhari, 2022). L’aumento considerevole delle procedure di elettrofisiologia e di cardiostimolazione degli ultimi anni e, in particolar modo, quelle di impianto di ILR/ICM dovute all’allargamento delle indicazioni al loro utilizzo, hanno inoltre recentemente indotto alcuni centri a considerare la possibilità di far eseguire agli infermieri anche le procedure di espianto sia degli ICM sia dei precedenti modelli di ILR.
OBIETTIVO
Obiettivo dello studio è esplorare la sicurezza dell’espianto di ILR e ICM da parte di infermieri appositamente formati.
METODI
È stato condotto uno studio osservazionale retrospettivo relativo agli eventi avversi peri-procedurali (ad es. emorragie, ematomi, infezioni) in una serie consecutiva di espianti di loop recorder eseguiti presso l’istituto di ricovero e cura a carattere scientifico (IRCCS) Centro Cardiologico Monzino di Milano (Italia) tra gennaio 2019 e gennaio 2021. Questo centro è un ospedale metropolitano, accreditato all’interno del Servizio Sanitario Nazionale, esclusivamente dedicato alle malattie cardiovascolari. In questo ospedale è stato stilato un protocollo, condiviso tra lo staff infermieristico, i medici elettrofisiologi e la direzione sanitaria, che coinvolge gli infermieri nella gestione dei pazienti con ILR o ICM dalla fase di impianto (Cervellione, 2018) a quella di follow-up, fino all’espianto e a un eventuale re-impianto del dispositivo.
Questo studio è stato autorizzato dal comitato scientifico e approvato dal “Comitato Etico degli IRCCS Istituto Europeo di Oncologia e Centro Cardiologico Monzino” di Milano.
Aspetti Metodologici
Sono stati inclusi nello studio tutti i pazienti consecutivi sottoposti a espianto di loop recorder da gennaio 2019 a gennaio 2021, a prescindere dalla condizione clinica del paziente.
Una volta recuperato l’elenco dei pazienti che sono stati sottoposti a espianto, si è provveduto a ricercare la cartella clinica informatizzata di ricovero per estrapolare le informazioni di interesse. Sono stati raccolti i seguenti dati: dati anagrafici (età e genere), dati clinico assistenziali (peso, altezza, BMI, assunzione di farmaci antiaggreganti e/o anticoagulanti), dati relativi alla procedura di espianto (tipo di ILR espiantato, operatore, posizione di inserimento del dispositivo, modalità di sutura, esecuzione di profilassi antibiotica se prescritta dal medico), complicanze (sanguinamento immediato o dopo 24 ore, ematoma a 10 giorni dall’impianto, infezione a 30 giorni dall’impianto), indicazioni all’impianto di ILR (tutte le principali aritmie e le patologie che possono provocare eventuali aritmie, quali la Sindrome di Brugada, o che possono indurre delle patologie secondarie, quali l’ictus criptogenetico), dati relativi alla possibilità di un eventuale reimpianto (tipo di dispositivo, operatore, modalità di sutura, complicanze al reimpianto).
Descrizione dei dispositivi espiantati
La maggior parte dei dispositivi utilizzati, e quindi espiantati, nel centro è costituita da ICM Medtronic Reveal LINQTM. Questo dispositivo è caratterizzato da un volume di soli 1.2 cc, ha un peso di 2.5 g, una distanza tra gli elettrodi di 38 mm, ha una durata di 3 anni e permette la registrazione di 59 minuti totali di episodi (rilevati automaticamente o attivati dal paziente). Altri dispositivi espiantati sono stati: ILR Medtronic Reveal XTTM con un volume di 9 cc, una distanza tra gli elettrodi di 40 mm, un peso di 15 g e una durata di 3 anni e infine ILR Biotronik Biomonitor 2AF con un volume di 5 cc, un peso di 10 g e una durata di 4 anni. La maggior parte dei dispositivi era stata impiantata in zona parasternale sinistra, a livello del 4°-5° spazio intercostale, con un’inclinazione di 45° rispetto al bordo dello sterno come da linee guida del costruttore (Figura 1).
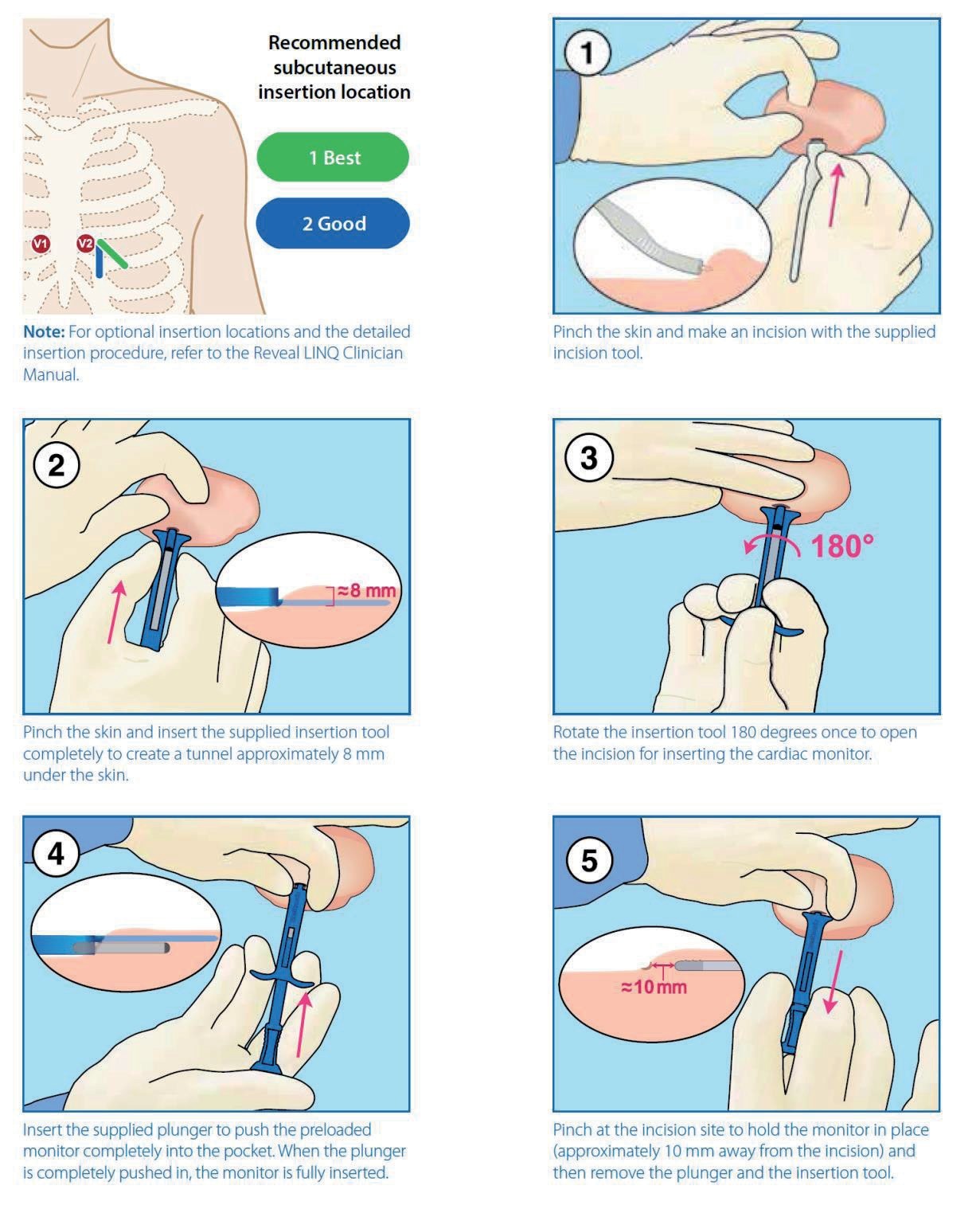
Figura 1. – Procedura di impianto dell’ICM tramite iniezione (Courtesy of Medtronic International Trading Sarl).
Procedura di gestione del paziente
Due infermieri sono stati formati da medici elettrofisiologi tramite un corso teorico e pratico durante il quale sono stati affrontati i seguenti temi: anatomia vascolare e cutanea del sito di accesso, gestione delle complicanze relative all’incisione della cute, fasi della procedura di impianto e fasi della procedura di espianto (Figura 1, 2) (Cervellione, 2018; Rogers, 2017). Dopo la formazione, ogni infermiere, è stato affiancato da un medico elettrofisiologo durante le prime tre procedure di impianto e le prime tre procedure di espianto dal vivo. Al termine del corso è stata fornita a ogni infermiere una scheda riepilogativa con le istruzioni di impianto ed espianto dell’ILR o ICM (Figura 1, 2) e, solo al completamento della sessione pratica e dopo approvazione del medico elettrofisiologo, ha ottenuto una certificazione per poter effettuare la procedura.

Figura 2. – Fasi di espianto dell’ICM (Courtesy of Medtronic International Trading Sarl).
La suddivisione delle attività tra personale medico e infermieristico presso il centro in ogni fase della procedura di espianto dell’ICM/ILR e dell’eventuale sostituzione è descritta nella tabella 1. Le procedure di espianto sono state effettuate sia da medici elettrofisiologi sia dagli infermieri certificati, nella sala di elettrofisiologia. La scelta del tipo di operatore (medico o infermiere) è stata fatta in base alla loro disponibilità. Nel caso di sostituzione dell’ILR con un altro CIED (pacemaker o defibrillatore) l’espianto dell’ILR è sempre stato fatto dal medico elettrofisiologo, che ha effettuato il successivo impianto di CIED nella stessa procedura. Prima dell’esecuzione della procedura di espianto è stata eseguita una terapia antibiotica profilattica (Bisignani, 2016). Nel caso in cui il paziente fosse in terapia farmacologica anticoagulante o antiaggregante questa non è stata interrotta prima della procedura di espianto. La procedura ha inizio con la rilevazione, nel sottocute, del dispositivo da espiantare e dell’esito cicatriziale cutaneo in modo da eseguire l’incisione della cute con la stessa lunghezza (8 mm) e in prossimità di quella eseguita per l’impianto. Si esegue l’infiltrazione, nello strato sottocutaneo e in particolare nella zona di incisione, di anestesia locale e, dopo essersi assicurati dell’avvenuta azione del farmaco, si passa all’incisione dello strato superficiale della cute con un bisturi a lama dritta. Con l’aiuto di una pinza Mosquito curva e una pinza vascolare chirurgica si passa a dissezionare gli strati sottostanti della cute fino ad incontrare la capsula di fibrina che avvolge il dispositivo. Tramite il bisturi la capsula viene incisa e il dispositivo viene estratto con l’aiuto della pinza vascolare chirurgica. Verificata la possibilità di eseguire eventuale emostasi si passa alla chiusura della ferita con l’applicazione di strisce adesive per la sutura cutanea e della medicazione avanzata. Nel caso di espianto con sostituzione di ILR, il nuovo dispositivo è stato inserito nella stessa posizione, a meno di problemi con la rilevazione del segnale nella posizione originale. Il nuovo ILR è stato poi attivato e programmato dall’infermiere per registrare, automaticamente, i parametri e gli eventi aritmici (fibrillazione atriale, pause, tachicardia o bradicardia ventricolare) in accordo alla programmazione del precedente dispositivo, alle indicazioni del medico elettrofisiologo e alla storia clinica attuale del paziente.
All’infermiere è affidata la comunicazione con i pazienti in caso di eventi avversi o per indicazioni su eventuali azioni da intraprendere (ad es. recarsi in pronto soccorso, prenotare visita cardiologica, effettuare trasmissioni ravvicinate).
| Attività | Medici Elettrofisiologi | Infermieri |
| Indicazione all’espianto o alla sostituzione con un nuovo ICM | R | |
| Esecuzione dell’espianto di ICM/ILR | R | R |
| Esecuzione dell’impianto del nuovo ICM | R | R |
| Attivazione del nuovo ICM | S | R |
| Programmazione del nuovo ICM | S | R |
| Registrazione del nuovo ICM al sistema di monitoraggio da remoto | R | |
| Formazione del paziente | R | |
| Triage iniziale sulla trasmissione dei dati da remoto | R | |
| Prescrizione di ulteriori esami e/o terapie | R | |
| Legenda
R= Responsabile; S= Supervisione ICM = Monitor cardiaco iniettabile; ILR = Loop recorder impiantabile
|
||
Tabella 1. – Schema relative alla suddivisione delle responsabilità per l’espianto, eventuale sostituzione e follow-up di ICM/ILR.
Analisi Statistiche
Le variabili continue sono state sintetizzate sotto forma di media e deviazione standard, mentre le variabili qualitative sono state presentate sotto forma di frequenza assoluta e relativa. I confronti tra i gruppi indipendenti sono stati effettuati utilizzando il test di Wilcoxon per le variabili continue e il test Chi-quadro per le variabili categoriche. Tutti i test svolti sono stati a 2 code e la significatività statistica è stata indicata attraverso un p-value <0,05. Le analisi sono state svolte attraverso il software Stata 12.1 (Stata Corp, College Station, TX).
RISULTATI
Tra gennaio 2019 e gennaio 2021, 202 pazienti (141 di sesso maschile, con età media di 58.95±17.6 anni, range 19 – 87 anni) sono stati sottoposti ad espianto ILR. Dei pazienti giunti per l’espianto, 90 (44,5%) avevano ricevuto l’ILR per il monitoraggio della fibrillazione atriale, 44 (21,8%) per sincopi ricorrenti di presunta origine cardiaca, 28 (13,9%) per sospetta tachicardia ventricolare, 10 (4,9%) per palpitazioni, 11 (5,4%) per sospetta Sindrome di Brugada, 10 (4,9%) per sospette pause, 4 (2%) per Ictus con sospetta derivazione da fibrillazione atriale e 5 (2,5%) per sospetta bradicardia. Ottantotto procedure di espianto (43.6%) sono state effettuate da medici elettrofisiologi, mentre le restanti 114 (56.4%) sono stati effettuate dai due infermieri. Tutte le procedure sono state effettuate nella sala di elettrofisiologia.
Le caratteristiche cliniche dei pazienti all’espianto stratificate in base alla tipologia di operatore che ha eseguito l’espianto, sono riportate in tabella 2. Centotredici (55.9%) pazienti assumevano anticoagulanti o antiaggreganti e non li hanno sospesi durante la procedura. I due gruppi sono confrontabili per le principali variabili indagate.
| TOTALE
(n= 202) |
Pazienti espiantati dal medico elettrofisiologo
(n=88; 43,6%) |
Pazienti espiantati dagli infermieri
(n=114; 56,4%) |
p-value
|
|
| Età (anni), Media ± DS | 58,9 ± 16,4 | 57,6 ± 17,0 | 60,0 ± 16,0 | 0,571 |
| Genere (Femmine), % (n) | 30,2 (61) | 32,9 (29) | 28,1 (32) | 0,339 |
| BMI, Media ± DS | 25,3 ± 3,7 | 25,3 ± 2,8 | 25,4 ± 4,2 | 0,903 |
| Terapia antibiotica preimpianto, % (n) | 100 (100) | 100 (88) | 100 (114) | — |
| Terapia anticoagulante/antiaggregante, % (n) | 55,9 (113) | 56,8 (50) | 55,3 (63) | 0,285 |
| Posizionamento dell’ICM a 45°, % (n) | 94,1 (190) | 95,5 (84) | 93,0 (106) | 1,000 |
| Nota
I numeri sono espressi come frequenze relative (assolute); I parametri su scala continua sono presentati come media ± deviazione standard. BMI = l’indice di massa corporea; ILR = loop recorder impiantabile.
|
||||
Tabella 2. – Caratteristiche del campione.
I dispositivi espiantati erano: 197 (97.5%) Medtronic Reveal LINQTM, 3 (1.5%) Medtronic Reveal XTTM e 2 (1%) Biotronik Biomonitor 2AF. Tali dispositivi erano stati impiantati con inclinazione di 45° rispetto al bordo dello sterno oppure posizione verticale parallela allo sterno (come consigliato dal produttore) in 193 pazienti (95.6%) e in posizione diversa in 9 (4.4%).
In 4 casi in cui il paziente era indicato alla sostituzione dell’ICM e il sensing medio non era ottimale (<0, 2 mV), il nuovo dispositivo non è stato iniettato nella tasca sottocutanea precedente ma nella posizione consigliata (45° rispetto al bordo dello sterno, a livello del 4°-5° spazio intercostale). Il sensing medio nella precedente tasca era 0,17 mV, mentre nella nuova posizione, misurato con il nuovo dispositivo, 0,65 mV.
Per la procedura di espianto, l’incisione della cute è stata eseguita tramite bisturi a lama dritta e successivamente richiusa tramite strisce adesive per la sutura cutanea (steri-strip) nella maggior parte dei casi (135 pazienti; 66.8%). Questo metodo di chiusura è stato utilizzato maggiormente dagli infermieri rispetto che dai medici elettrofisiologi (84.2% vs. 35.2%; p<0,001), mentre la chiusura tramite clips metalliche è stata utilizzata maggiormente dai medici elettrofisiologi che dagli infermieri (47.7% vs. 7%; p<0,001), così come la sutura con filo (15.9% dai medici vs. 2.6% dagli infermieri; p=0,007). Sono state riscontrate differenze nel tempo di espianto medio tra le procedure eseguite dai medici elettrofisiologi e quelle eseguite dagli infermieri (11,5±1.9 minuti vs 14,5±2,2 minuti; p<0,001).
Il tasso di successo degli espianti è stato pari al 100% con entrambe le tipologie di operatore. Per nessun paziente si sono verificati eventi avversi seri durante la procedura o nei 30 giorni successivi. Due episodi (1%) di sanguinamento minore sono avvenuti al termine di procedure di espianto effettuate dagli infermieri, ma sono stati rapidamente risolti dagli stessi tramite digitopressione. I 5 ILR non iniettabili (3 Medtronic Reveal XTTM, 2 Biotronik Biomonitor 2AF) sono stati espiantati 2 dagli infermieri e 3 dai medici elettrofisiologi; per entrambi i gruppi non ci sono stati eventi avversi.
DISCUSSIONE
È già stato mostrato che un protocollo gestionale che consenta il primo impianto di ILR da parte di infermieri debitamente formati e la delega agli infermieri delle altre attività associate a questo dispositivo, incluso il follow-up remoto (BHRS, 2018), è sicuro e apporta benefici sia al paziente sia alla struttura sanitaria (Roebuck, 2015; Wong, 2016). Il nostro studio sembra suggerire che la responsabilità degli infermieri appositamente formati può essere estesa anche all’espianto dell’ILR e all’eventuale re-impianto.
Nonostante la procedura di espianto possa essere percepita come chirurgicamente più invasiva rispetto all’impianto dell’ICM (che, grazie agli strumenti dedicati presenti nella confezione, è molto simile a un’iniezione), questa è risultata sicura anche quando effettuata dagli infermieri. Nella nostra esperienza l’incidenza di complicanze è stata dell’1%, valore confrontabile con quello degli impianti effettuati dagli infermieri in altri studi (Cervellione, 2018; Eftekhari, 2022). Rispetto allo studio di Lim et al. (2019), nella nostra esperienza non ci sono state infezioni. Non si può escludere che questo sia legato al fatto che tutti gli impianti sono stati effettuati in sala di elettrofisiologia e con profilassi antibiotica.
Il processo di miniaturizzazione del dispositivo ha reso l’espianto dell’ICM fattibile da parte degli infermieri e sicuro per la maggior parte dei pazienti, indipendentemente da fattori fisici o biologici quali l’età o l’anatomia. Come in altre esperienze pubblicate (Lim, 2019; Eftekhari, 2022), la sutura dell’incisione tramite steri-strip è stata quella preferibilmente utilizzata, da parte degli infermieri, poiché risulta estremamente semplice da eseguire ed evita qualsiasi restrizione a letto o limitazione nei movimenti del paziente, consentendo quindi la completa indipendenza dei pazienti nelle loro attività quotidiane subito dopo l’espianto.
Il tempo medio necessario per la procedura di espianto degli ICM è risultato inferiore ai 15 minuti ed è paragonabile a quello delle procedure di impianto (Cervellione, 2018; Lim, 2019; Di Odoardo, 2017; Kanters, 2016), nella nostra esperienza il medico elettrofisiologo è riuscito a completare l’espianto circa 3 minuti prima dell’infermiere, questo può essere dovuto dalla maggior esperienza maturata nella tecnica. La possibilità di delegare agli infermieri anche in questo tipo di procedura consente di distribuire al meglio il carico di lavoro tra diverse tipologie di operatore sanitario, in base al diverso livello di complessità di ciascuna attività (Roebuck, 2015; Kanters, 2016).
Per aumentare i benefici relativi all’ottimizzazione delle risorse dell’ospedale, si può considerare di far effettuare anche questo tipo di procedura agli infermieri in ambienti alternativi alla sala di elettrofisiologia, come già accade per il primo impianto di ILR/ICM (Cervellione, 2018; Wong, 2016; Kanters, 2016). Un esempio è la sala risveglio (Cervellione, 2018), che è un ambiente costantemente sanificato (BHRS, 2018), con monitor defibrillatore, monitor per la rilevazione dei parametri vitali, postazione del letto con presenza di attacchi per gas e vuoto; ed essendo, questa, attigua alle sale interventistiche dà la possibilità di una pronta presenza del medico elettrofisiologo in caso di emergenza. È già stato mostrato che la procedura di espianto in questo tipo di ambiente può essere effettuata senza complicanze peri-procedurali da parte del medico elettrofisiologo (Yarlagadda, 2018). Inoltre, si sta studiando la possibilità di inserire ambedue le procedure come attività svolte ambulatorialmente così come succede in altri contesti internazionali (Roebuck, 2015; Wong, 2016; Yarlagadda, 2018).
Nell’esperienza del nostro centro, affidando anche l’espianto dell’ILR agli infermieri è stato possibile migliorare ulteriormente l’allocazione delle risorse ospedaliere, permettendo ai medici elettrofisiologi di svolgere procedure più complesse. Questo si è rivelato particolarmente importante nel periodo di osservazione dello studio, poiché la pandemia di COVID-19 ha contingentato ulteriormente il personale medico ed è stato essenziale l’apporto degli infermieri per l’impianto, il follow-up e l’espianto degli ILR.
Il coinvolgimento della figura dell’infermiere nell’ impianto, follow-up ed espianto o sostituzione dell’ILR/ICM, in base ad uno specifico schema di suddivisione delle responsabilità e in collaborazione con gli specialisti in elettrofisiologia, consente agli infermieri di ampliare le proprie responsabilità e di accrescere le competenze professionali.
Limiti dello studio
Questo articolo riporta l’esperienza di un singolo centro. L’assegnazione dei pazienti è dipesa dalla disponibilità dell’operatore al momento della procedura, all’organizzazione della sala e degli ambulatori e alla necessità dell’impianto concomitante di altro CIED durante la stessa procedura. Pertanto, i due gruppi potrebbero non essere bilanciati rispetto ad alcune caratteristiche di base o comorbidità che non sono state indagate. Sono necessari altri studi, con approcci metodologici differenti e su campioni più numerosi per confermare che il tasso di complicanze dell’espianto eseguito in sala di elettrofisiologia dall’infermiere non sia superiore rispetto all’espianto effettuato dal medico elettrofisiologo.
CONCLUSIONI
Sebbene si rendano necessarie maggiori evidenze al fine di proporre la strategia illustrata come standard of care, questo studio suggerisce che gli infermieri formati possono eseguire autonomamente e in sicurezza un espianto di ICM/ILR senza necessità di risorse aggiuntive con benefici per il paziente, per la struttura sanitaria e per il personale ospedaliero.
Conflitto di interessi
Tutti gli autori dichiarano l’assenza di conflitto di interessi. Tutti gli autori dichiarano di aver contribuito alla realizzazione del manoscritto e ne approvano la pubblicazione.
Finanziamenti
Gli autori dichiarano di non aver ottenuto alcun finanziamento e l’assenza di sponsor economici.
Ringraziamenti
L’autore ringrazia Claudia Franzoni, Andrea Ghelfi, Giovanni Pensa, Paolo Rota e Annamaria Varbaro per il supporto tecnico e scientifico.




