RIASSUNTO
Introduzione Nei soggetti anziani con disturbi neurocognitivi il rischio di cadute è almeno doppio rispetto a quello osservato nei coetanei senza sintomi neurocognitivi. Nonostante la rilevanza clinica del problema, la conoscenza dell’efficacia degli interventi di prevenzione delle cadute in questa popolazione è limitata. L’obiettivo dello studio è valutare l’efficacia degli interventi di prevenzione delle cadute in soggetti con disturbi neurocognitivi.
Materiali e metodi E’ stata effettuata una overview di revisioni sistematiche con interrogazione di sette database biomedici. Le caratteristiche e i risultati principali degli studi eleggibili che hanno rispettato i criteri di inclusione sono stati analizzati e sintetizzati in tabelle sinottiche.
Risultati L’effetto degli interventi sulla riduzione del numero di cadute e del numero di soggetti caduti è modesto e occorrono ulteriori conferme. Le prove a sostegno dell’efficacia in termini di mortalità, numero di lesioni e numero di fratture sono insufficienti.
Conclusioni Allo stato attuale c’è molta incertezza sull’efficacia degli interventi di prevenzione delle cadute in soggetti adulti con disturbi neurocognitivi. Occorre descrivere e chiarire meglio le caratteristiche degli interventi, a quali particolari sottogruppi o setting sono destinati, l’accettabilità e il rapporto costo-efficacia.
Parole chiave: cadute, disturbi neurocognitivi, overview, revisioni sistematiche
Effectiveness of interventions to prevent falls in subjects with neurocognitive disorders. Overview of systematic reviews
ABSTRACT
Introduction In elderly subjects with neurocognitive disorders the risk of falls is at least twice that observed in peers without neurocognitive symptoms. Despite the clinical relevance of problem, the knowledge of effectiveness of fall prevention interventions in this population is limited. This study aims to evaluate efficacy falls prevention interventions in subjects with neurocognitive disorders.
Materials and methods An overview of systematic reviews was carried out with querying of seven biomedical databases. The characteristics and main results of eligible studies that met inclusion criteria were analyzed and synthesized in synoptic tables.
Results The effect of interventions on reducing the number of falls and the number of fallen subjects is low and further confirmation is needed. The evidence supporting efficacy in terms of mortality, number of injuries and number of fractures is insufficient.
Conclusions Currently there is much uncertainty about the effectiveness of falls prevention interventions in adults subject with neurocognitive disorders. It is necessary to better describe and clarify characteristics of interventions, for which particular subgroups of subjects or settings are appointed, the acceptability and the cost-effectiveness.
Keywords: falls, neurocognitive disorders, overview, systematic reviews
![]()
INTRODUZIONE
Le cadute dell’anziano sono un problema di salute pubblica per l’alta incidenza, le morbilità associate, le conseguenze psicosociali e i costi relativi. A partire dai 75 anni sono una delle maggiori cause di disabilità e la principale causa di mortalità (Härlein J et al., 2009; NICE, 2015). I fattori causali sono di natura multifattoriale e si dividono in estrinseci e intrinseci: questi ultimi dipendono da genere, età, stato di salute generale e livello di fragilità (Cox J et al., 2015; Wynaden D et al., 2016). Nei soggetti anziani la demenza e i disturbi neurocognitivi sono da tempo riconosciuti fra i principali fattori di rischio intrinseci di cadute: la prevalenza in persone di oltre 65 anni è circa il 5% e sale al 30% nei soggetti con più di 80 anni (Shaw FE, 2002; Härlein J et al., 2009). Si stima che il rischio di cadute negli anziani con deficit neurocognitivo sia da due a tre volte superiore rispetto a quello rilevato in anziani neurocognitivamente integri, con un’incidenza annuale del 60-80% (Härlein J et al., 2009). Nei soggetti con deficit neurocognitivo la prognosi è peggiore e la probabilità di un buon recupero funzionale minore (Härlein J et al., 2009). E’ opinione diffusa che qualsiasi forma di prevenzione sia difficile da attuare in questi soggetti (Shaw FE, 2002; Wynaden D et al., 2016). Tuttavia la valutazione di efficacia degli interventi di prevenzione delle cadute nei soggetti a rischio di caduta come quelli con disturbi neurocognitivi deve costituire per gli operatori e le organizzazioni sanitarie un argomento di interesse prioritario (Härlein J et al., 2009; Wynaden D et al., 2016). Molti studi sono centrati su persone neurocognitivamente integre o prendono in esame interventi di prevenzione standardizzati su una popolazione eterogenea (Härlein J et al., 2009; Cox J et al., 2015). Ciò comporta che, nonostante la rilevanza clinica del problema, la conoscenza sull’efficacia degli interventi di prevenzione delle cadute in soggetti con disturbi neurocognitivi sia limitata.
Obiettivo
Lo studio si pone l’obiettivo di valutare l’efficacia degli interventi di prevenzione delle cadute in soggetti con disturbi neurocognitivi.
MATERIALI E METODI
Disegno dello studio
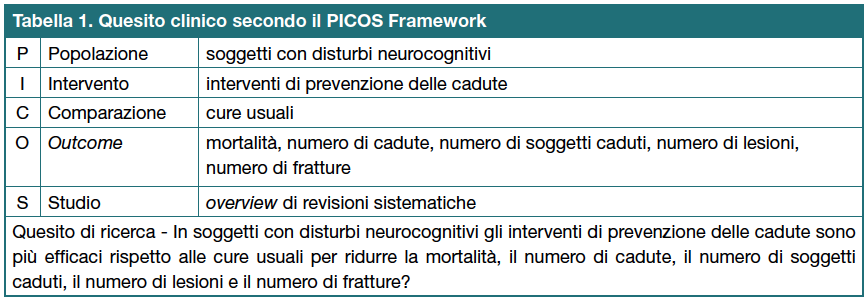
E’ stata condotta una overview di revisioni sistematiche per sintetizzare le migliori prove di efficacia disponibili e definire le opportune decisioni cliniche e assistenziali (Cooper H et al., 2012). Il quesito di ricerca è stato strutturato di comune accordo fra gli autori secondo il PICOS Framework (Robinson KA et al., 2011; Tabella 1).
Strategia di ricerca
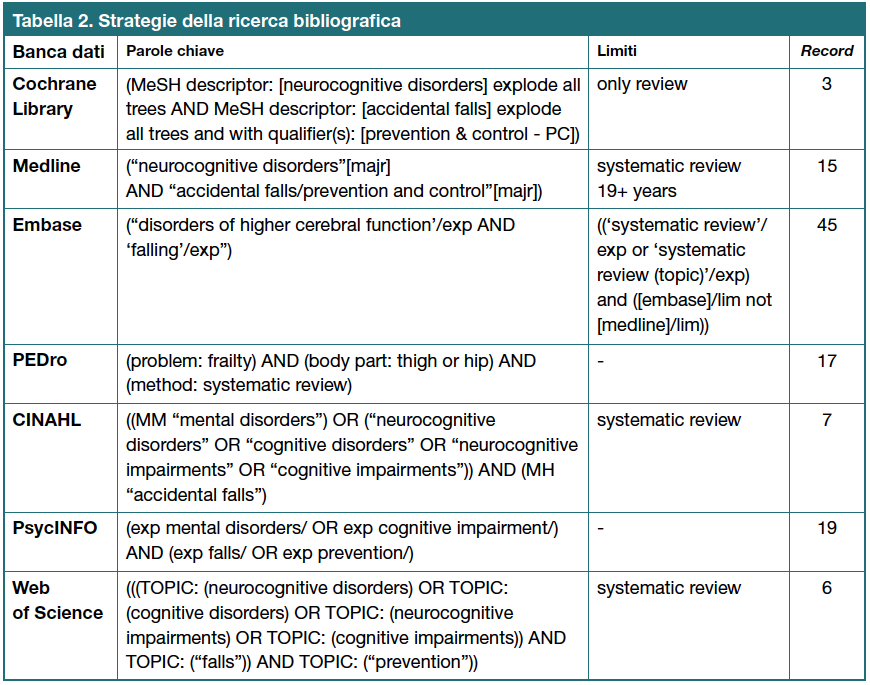
Per la ricerca dei documenti di interesse il primo autore (LGR), previa discussione e accordo con il secondo (ML) sulle parole chiave da adottare, ha implementato su sette database elettronici (The Cochrane Library, Medline, Embase, PEDro, CINAHL, PsycINFO, Web of Science) il 13 Gennaio 2017 una strategia di ricerca per termini MeSH, Subheadings e/o parole a testo libero (Tabella 2).
In modo indipendente il secondo autore (ML) ha applicato una strategia di ricerca basata sulle stesse parole chiave e tramite confronto dei risultati per le situazioni controverse si è raggiunto un accordo comune. Non sono stati applicati criteri di esclusione in base a lingua o data di pubblicazione. Non è stata esaminata la letteratura non pubblicata o in fase di pubblicazione né sono stati contattati degli esperti clinici per il recupero di altre fonti. L’analisi e la selezione dei record per titolo e abstract è avvenuta in modo indipendente, prima dal primo autore (LGR) poi dal secondo (ML). Ogni citazione è stata vagliata per pertinenza e rilevanza; in caso di informazioni insufficienti per dare un giudizio definitivo, prima di deciderne l’esclusione, è stato reperito il documento full text e analizzato da ambedue gli autori (LGR e ML). Le revisioni selezionate hanno dovuto rispettare i criteri di inclusione previsti. La bibliografia delle revisioni sistematiche eleggibili è stata analizzata dal primo autore (LGR) e successivamente ricontrollata dal secondo autore (ML) per recuperare altri studi di potenziale interesse. Qualsiasi controversia è stata affrontata e risolta di comune accordo.
Criteri di selezione degli studi
Sono state incluse le revisioni sistematiche con o senza metanalisi di sperimentazioni cliniche controllate randomizzate (RCT) o di studi quasi sperimentali. Sono stati presi in esame adulti con disturbi neurocognitivi istituzionalizzati (per esempio in ospedale o in unità di cure a lungo termine) o non istituzionalizzati. Sono state escluse le revisioni condotte su soggetti senza disturbi neurocognitivi e quelle su popolazione mista a meno che non fosse possibile valutare l’efficacia degli interventi in funzione dello stato neurocognitivo per la presenza di dati aggregati. Gli interventi di interesse sono stati quelli di prevenzione delle cadute confrontati con le cure usuali. Sono state ritenute eleggibili le revisioni con dati o informazioni in merito ai seguenti esiti: mortalità, numero di cadute, numero di soggetti caduti, numero di lesioni, numero di fratture.
Valutazione della qualità metodologica
La qualità e il rigore metodologico delle revisioni incluse sono stati valutati in modo indipendente dai due autori (LGR e ML) con l’AMSTAR Checklist (Shea BJ et al., 2007). Con punteggio pari a 8-11, 4-7 e 0-3 è stata assegnata rispettivamente alta, moderata o bassa qualità (Ryan R et al., 2014). Il parere del secondo autore è stato vincolante in caso di dubbio sull’attribuzione del punteggio.
Estrazione dei dati
Sono state estratte e riportate in una tabella sinottica dal primo autore (LGR) e ricontrollate dal secondo autore (ML) le seguenti informazioni: primo autore e anno della revisione, qualità metodologica della revisione, numero di studi inclusi e loro qualità metodologica (in funzione dello strumento di valutazione adottato dai loro autori), obiettivo, numero di partecipanti, età media, livello di disturbo neurocognitivo, setting di reclutamento, tipologia di intervento e controllo, esiti e risultati principali. Dubbi o controversie sono state risolte dopo un confronto e il raggiungimento del consenso comune.
RISULTATI
Esiti della strategia di ricerca
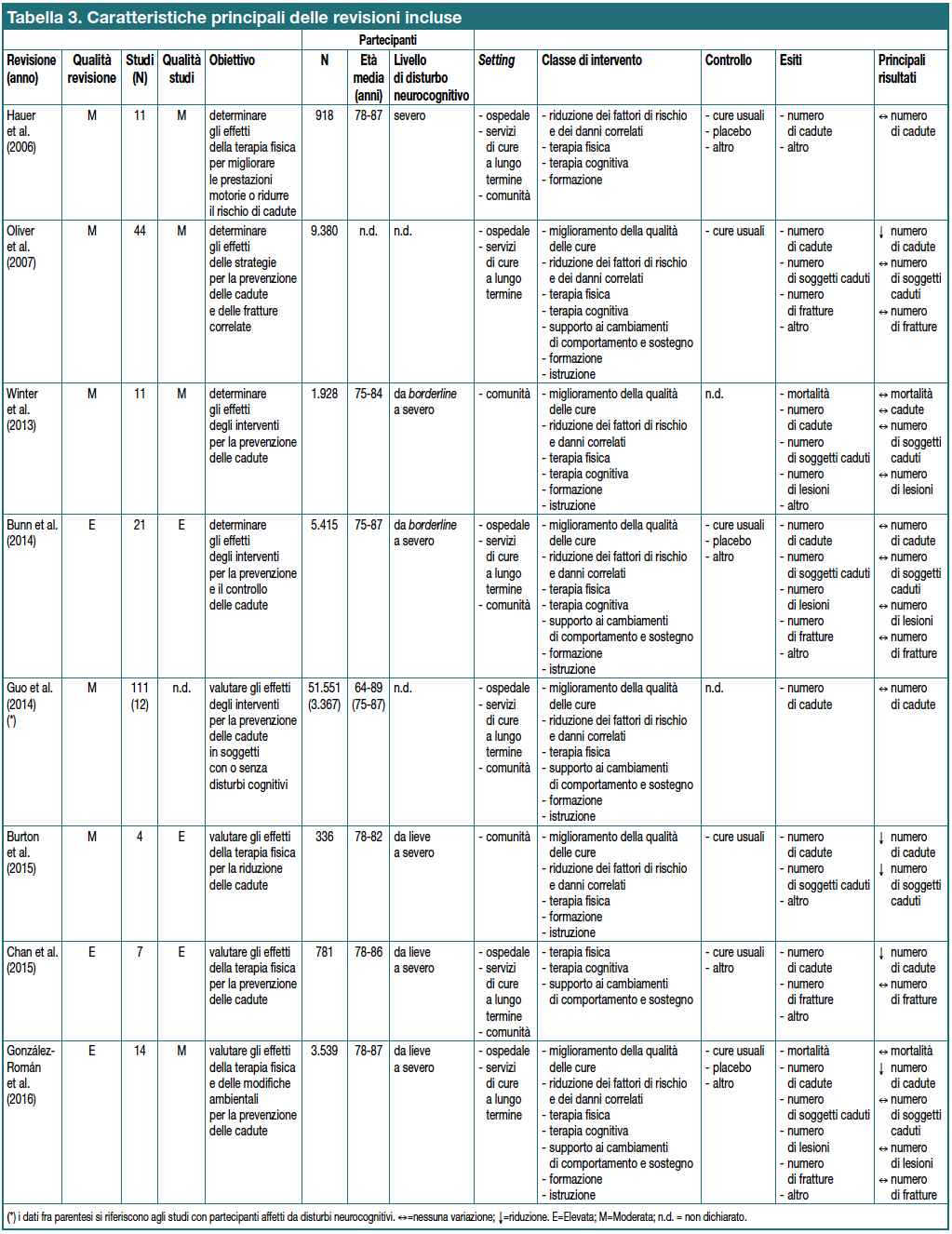
La strategia di ricerca, al netto di 13 duplicati, ha identificato 99 record dei quali ne sono stati esclusi 88 dopo lettura di titolo e abstract (13 non erano pertinenti all’argomento, 75 non rispettavano uno o più criteri di inclusione). Degli 11 record restanti, valutati per eleggibilità, sono stati reperiti i documenti in full text e su questi è stata eseguita un’analisi della bibliografia per individuare altre citazioni di interesse, il che ha condotto all’identificazione di ulteriori 10 studi potenzialmente eleggibili. Tutti e 21 i documenti sono stati analizzati per verificare i criteri di inclusione. Il processo ha comportato l’esclusione: di cinque studi perché non rispettavano uno o più criteri di inclusione (Hill-Westmoreland EE et al., 2002; Heyn P et al., 2004; Härlein J et al., 2007; Jensen LE et al., 2011; Meyer C et al., 2015); di due studi in quanto presentavano dati aggregati su partecipanti con o senza disturbi neurocognitivi (Cameron ID et al., 2012; Gillespie LD et al., 2012) e di altri sei dal momento che non esplicitavano chiaramente la presenza di partecipanti con disturbi neurocognitivi (Chang JT et al., 2004; Clemson L et al., 2008; Coussement J et al., 2008; Sherrington C et al., 2008; El-Khoury F et al., 2013; Silva RB et al., 2013). Complessivamente sono state incluse otto revisioni sistematiche (Hauer K et al., 2006; Oliver D et al., 2007; Winter H et al., 2013; Bunn F et al., 2014; Guo JL et al., 2014; Burton E et al., 2015; Chan WC et al., 2015; Gonzàlez-Romàn L et al., 2016) che coprono un arco temporale di dieci anni. Di queste cinque sono con metanalisi (Oliver D et al., 2007; Guo JL et al., 2014; Burton E et al., 2015; Chan WC et al., 2015; Gonzàlez-Romàn L et al., 2016). In Tabella 3 sono descritte le caratteristiche principali delle revisioni incluse.
Qualità metodologica e caratteristiche delle revisioni incluse
Nel complesso la qualità metodologica è da moderata a elevata (punteggio AMSTAR da 6 a 9). Gli studi inclusi sono 124, di questi 89 (72%) sono RCT. Ventotto studi controllati (31%) sono comuni a due o più revisioni. Sei revisioni sistematiche (Hauer K et al., 2006; Oliver D et al., 2007; Bunn F et al., 2014; Burton E et al., 2015; Chan WC et al., 2015; Gonzàlez-Romàn L et al., 2016) riportano lo strumento utilizzato per la valutazione della qualità metodologica degli studi inclusi e ne presentano i risultati.
Una revisione (Winter H et al., 2013) analizza il disegno di studio, i criteri di selezione, le dimensioni del campione, i fattori confondenti, le perdite al follow up; un’altra (Guo JL et al., 2014) non prevede l’utilizzo esplicito di criteri formali o informali di valutazione della qualità.
Generalmente la qualità metodologica degli studi primari è da moderata ad elevata; i bias che ricorrono più di frequente sono:
- attrition bias (per esempio soggetti persi al follow up; Hauer K et al., 2006; Burton E et al., 2015);
- detection bias (per esempio cecità dei valutatori; Bunn et al., 2014);
- performance bias (per esempio cecità dei partecipanti e degli operatori; Chan WC et al., 2015; Gonzàlez-Romàn L et al., 2016);
- information bias (per esempio misclassificazione dei partecipanti; Hauer K et al., 2006).
Il numero di soggetti con disturbi neurocognitivi inclusi nelle revisioni è compreso fra 336 (Burton E et al., 2015) e 5.415 (Bunn F et al., 2014). L’età media è compresa fra 75 e 87 anni. In tutte le revisioni, tranne in due (Oliver D et al., 2007; Guo JC et al., 2014), è indicato lo stato cognitivo dei partecipanti, valutato prevalentemente con il Mini-Mental State Examination (MMSE) o lo Short Portable Mental Status Questionnaire (SPMSQ).
Il grado di disturbo cognitivo rilevato è da border line a severo. Quattro revisioni includono soggetti istituzionalizzati e non istituzionalizzati (Hauer K et al., 2006; Bunn F et al., 2014; Guo JC et al., 2014; Chan WC et al., 2015), due includono esclusivamente soggetti istituzionalizzati (Oliver D et al., 2007; Gonzàlez-Romàn L et al., 2016) e due esclusivamente partecipanti non istituzionalizzati (Winter et al., 2013; Burton et al., 2015). Gli interventi applicati sono ampiamente eterogenei: in alcuni casi si tratta di interventi singoli mentre in altri di più interventi, erogati contemporaneamente o in successione cronologica fra loro. Ogni intervento può essere incluso essenzialmente in una delle seguenti classi:
- miglioramento della qualità delle cure;
- riduzione dei fattori di rischio e dei danni correlati;
- terapia fisica (intesa come regime o piano di attività fisica progettato e prescritto per ripristinare una ottimale funzionalità muscolo-scheletrica);
- terapia cognitiva (intesa come forma diretta di psicoterapia basata sull’interpretazione di situazioni che determinano come un individuo si sente e si comporta e che utilizza tecniche comportamentali/verbali per identificare e correggere il pensiero negativo alla radice del comportamento aberrante migliorando o potenziando le abilità di attenzione, percezione, movimento, memoria, linguaggio, pensiero);
- supporto ai cambiamenti di comportamento e sostegno psicologico (al paziente e/o al caregiver e/o al team di cura);
- formazione, intesa come processo di affinamento di competenze e capacità (al paziente e/o al caregiver e/o al team di cura);
- istruzione, intesa come processo di trasmissione di conoscenze (al paziente e/o al caregiver e/o al team di cura).
Sei revisioni (Oliver D et al., 2007; Winter H et al., 2013; Bunn F et al., 2014; Guo JC et al., 2014; Burton E et al., 2015; González-Román L et al., 2016) valutano l’efficacia degli interventi di miglioramento della qualità delle cure (per esempio approccio multidisciplinare alle cure, programma personalizzato di interventi, assistenza infermieristica individualizzata), sette revisioni valutano (Hauer K et al., 2006; Oliver D et al., 2007; Winter H et al., 2013; Bunn F et al., 2014; Guo JC et al., 2014; Burton E et al., 2015; González-Román L et al., 2016) l’effetto degli interventi di riduzione dei fattori di rischio e dei danni correlati (per esempio valutazione clinica e assistenziale approfondita, stratificazione dei soggetti per livello di rischio, controllo e gestione delle comorbilità, degli stati di malnutrizione o disidratazione potenziali o accertati, controllo dell’uso di farmaci psicotropi o antipertensivi o diuretici, dei mezzi di contenzione fisici e/o chimici, valutazione dei deficit funzionali e/o sensoriali, dell’ambiente di vita, dell’abbigliamento, delle calzature, della cura dei piedi, uso dei presidi per la deambulazione, dei dispositivi come i protettori dell’anca, del supporto farmacologico con calcio e vitamina D); tutte le revisioni valutano l’efficacia della terapia fisica (esercizi eseguiti individualmente o a piccoli gruppi di resistenza, forza, mobilità, flessibilità, coordinazione, equilibrio; esercizi di tipo isotonico e/o isometrico, anaerobico e/o aerobico, da eseguire durante la marcia, in piedi, seduti, con o senza ausili). Sei revisioni (Hauer K et al., 2006; Oliver D et al., 2007; Winter H et al., 2013; Bunn F et al., 2014; Chan WC et al., 2015; González-Román L et al., 2016) valutano il beneficio della terapia cognitiva (stimolazione unisensoriale, per esempio aromaterapia, o multisensoriale, per esempio snoezelen room individuale o a piccoli gruppi, interazione verbale o sociale individuale o di gruppo con attività ricreative), cinque revisioni valutano (Oliver D et al., 2007; Bunn F et al., 2014; Guo JC et al., 2014; Chan WC et al., 2015, González-Román L et al., 2016) l’efficacia di interventi di supporto ai cambiamenti di comportamento (per esempio potenziamento delle abilità di gestione delle attività di vita quotidiana) e interventi di sostegno psicologico (con sessioni individuali o di gruppo); sette revisioni misurano (Hauer K et al., 2006; Oliver D et al., 2007; Winter H et al., 2012; Bunn F et al., 2014; Guo JC et al., 2014; Burton E et al., 2015; González-Román L et al., 2016) l’effetto di interventi di formazione e/o istruzione (per esempio lezioni individuali, a diadi, a piccoli gruppi, frontali o interattive; brochure, materiale multimediale).
Gli interventi applicati sono singoli (per esempio esercizi di equilibrio), multipli (per esempio esercizi di forza, resistenza ed equilibrio), multisfaccettati (per esempio attività fisica e stimolazione neurosensoriale), multifattoriali (per esempio attività di miglioramento della qualità delle cure con gestione dei fattori di rischio e riduzione dei danni correlati). Le sessioni di intervento durano da 20 a 150 minuti con frequenza da bigiornaliera a mensile; la durata complessiva degli interventi è compresa fra due settimane e due anni. Gli operatori sanitari più di frequente coinvolti negli interventi sono medici, fisioterapisti, infermieri, terapisti occupazionali, dietisti e farmacisti.
Tutte le revisioni valutano l’effetto degli interventi sul tasso o sul numero di cadute dopo l’implementazione degli interventi: cinque revisioni (Oliver D et al., 2007; Winter H et al., 2013; Bunn F et al., 2014; Burton E et al., 2015; González-Román L et al., 2016) valutano il numero e/o la percentuale di soggetti caduti, altre cinque (Oliver D et al., 2007; Winter H et al., 2013; Bunn F et al., 2014; Chan WC et al., 2015; González-Román L et al., 2016) prendono in esame il numero di fratture e/o di lesioni e due revisioni (Winter H et al., 2013; González-Román L et al., 2016) la mortalità. Fra gli altri esiti presenti nelle revisioni a titolo di esempio vi sono il tasso di incidenza annuo di cadute o il numero di cadute per soggetto, il tasso o il numero di soggetti che sono caduti più di una volta, il tasso di incidenza annuo di fratture ogni mille soggetti, indicatori qualitativi o quantitativi di abilità motoria o cognitiva e la valutazione della qualità di vita percepita.
Effetto degli interventi per prevenire le cadute
Non è stato possibile illustrare l’efficacia degli interventi di prevenzione delle cadute sintetizzando i risultati in funzione di:
- età dei partecipanti;
- livello di disturbo neurocognitivo;
- omogeneità di classe di appartenenza degli interventi;
- grado di complessità della loro implementazione;
- setting di reclutamento.
Ciò perché nelle revisioni incluse viene misurato l’effetto ottenuto da più interventi o classi di intervento secondo criteri di aggregazione differenti fra i diversi studi. Per tale motivo ci si può lecitamente soffermare solo sul beneficio che gli interventi in generale hanno manifestato nei confronti di un definito esito. Cinque revisioni (Oliver D et al., 2007; Guo JC et al., 2014; Burton F et al., 2015; Chan WC et al., 2015; González-Román L et al., 2016) registrano un modesto effetto degli interventi sul tasso o sul numero di cadute mentre per 3 revisioni (Hauer K et al., 2006; Winter H et al., 2013; Bunn F et al., 2014) le prove di efficacia sono insufficienti; solo una (Burton E et al., 2015) descrive qualche beneficio sul numero di soggetti caduti. Per tutte le revisioni le prove di efficacia degli interventi sulla mortalità e sul numero di lesioni o di fratture sono insufficienti.
DISCUSSIONE
I risultati delle revisioni sistematiche incluse sono inconcludenti nel dimostrare un effetto significativo degli interventi per prevenire le cadute in soggetti con disturbi neurocognitivi.
Implicazioni per la pratica
Il problema dell’efficacia degli interventi per la prevenzione delle cadute in individui con disturbi neurocognitivi è ancora irrisolto (Chan WC et al., 2015). Nella pratica clinica viene suggerito di trattare i soggetti con grado di disturbo lieve secondo quanto definito dalle prove di efficacia per pazienti neurocognitivamente integri (Jensen J et al., 2003; Shaw FE, 2007). In carenza di prove dirette (Shaw FE, 2007), sembra che al peggiorare della condizione neurocognitiva diminuiscano gli effetti di interventi singoli o multipli (Vlaeyen E et al., 2015) a favore di quelli multisfaccettati o multifattoriali (Jensen J et al., 2003; Gonzàlez-Romàn L et al., 2016). Tuttavia, aumentando la complessità di questi ultimi si riduce l’efficacia, per una minore aderenza dei partecipanti (Jensen J et al., 2003) e un’attenzione subottimale alle caratteristiche individuali (Vlaeyen E et al., 2015). Secondo alcuni autori (Vlaeyen E et al., 2015; Gonzàlez-Romàn et al., 2016) non dovrebbe sorprendere che un approccio unico o con interventi singoli non dimostri beneficio, considerando l’eziologia complessa e multifattoriale del rischio di cadute, oltre all’insieme di fattori di rischio degli individui con deterioramento neurocognitivo (Jensen J et al., 2003; Shaw FE, 2007). Per comprendere l’impatto e i limiti degli interventi e facilitare i confronti fra gli studi occorre descrivere e chiarire meglio quali interventi o quali elementi siano efficaci, per quali sottogruppi di soggetti e/o per quali setting (Vlaeyen E et al.; 2015; Gonzàlez-Romàn L et al., 2016), l’accettabilità e il rapporto costo-efficacia (Bunn F et al., 2014).
Implicazioni per la ricerca
Bisogna compiere ricerche organizzate in base al setting di cura, alle caratteristiche e ai livelli di disturbo neurocognitivo per valutare l’effetto di interventi di accertata qualità che siano oltre che applicabili anche personalizzabili (Shaw FE, 2007; Neyens JC et al., 2011). Occorre ricordare che interventi non implementati secondo quanto pianificato, mal rispettati, che incontrano ostacoli nella pratica clinica quotidiana, che richiedono lavoro extra senza risorse materiali, umane e formative adeguate difficilmente hanno un effetto positivo, anche se potrebbero avere il potenziale per essere efficaci (Neyens JC et al., 2011). Per migliorare il tasso di successi sarebbero preferibili programmi di intervento multisfaccettati o multifattoriali erogati da un team multidisciplinare che abbia doti di coordinamento e comunicazione ottimali e in presenza di un buon livello di complementarietà e continuità delle cure (Neyens JC et al., 2011).
Limiti
Limiti della overview
Il reperimento dei documenti di interesse è avvenuto con una strategia di ricerca per termini MeSH e Subheadings e con una ricerca complementare o alternativa (in funzione delle caratteristiche proprie del database consultato) a testo libero, senza consultare la letteratura in fase di pubblicazione o non pubblicata né contattando esperti clinici. Questa scelta, meno dispendiosa in termini di tempo, potrebbe avere escluso documenti rilevanti; a parziale compenso di ciò sono stati interrogati sette database elettronici senza limiti temporali o di lingua di pubblicazione.
Limiti delle revisioni e degli studi inclusi
Le revisioni sistematiche incluse mostrano un’ampia eterogeneità per caratteristiche come qualità metodologica degli studi inclusi, criteri di inclusione, popolazione bersaglio, tipologia di interventi e controlli, setting, esiti di interesse, modalità di sintesi, presentazione e discussione dei risultati.
Molto variabile è anche il numero di partecipanti. Spesso il campione è sottodimensionato, anche per oggettive difficoltà di reclutamento, per poter rilevare effetti statisticamente significativi dovuti agli interventi.
Non vi è una chiara definizione dei casi: fra i partecipanti di alcuni studi vi sono sia soggetti cognitivamente integri sia con disturbi neurocognitivi; questo aspetto e la mancanza di analisi per sottogruppi in base al livello di disturbo neurocognitivo può influenzare l’esito degli interventi, condizionare la generalizzabilità dei risultati e rendere più difficile il confronto.
Alcuni studi prendono in esame solo interventi singoli, in altri studi tali interventi sono anche o esclusivamente una componente di interventi multisfaccettati o multifattoriali. Questi ultimi sono molto diversi per tipologia, numero, sequenza e scansione temporale di applicazione e per ruolo assunto da ogni singolo intervento. Ciò rende difficile riconoscere lo specifico beneficio determinato da ogni componente. Raramente sono proposti interventi o programmi di intervento specifici per le caratteristiche individuali e personalizzati in funzione del tipo, livello ed evoluzione del disturbo neurocognitivo. L’aderenza subottimale (a causa per esempio di problemi di salute, perdita di memoria, confusione, comportamento agitato o paranoico, mancanza di supporto da parte degli operatori sanitari e/o del caregiver o di sostegno sociale per condurre o proseguire con successo il trattamento) è un altro problema, insieme all’elevato tasso di abbandono. Inoltre si registrano alte perdite ai follow up (causate principalmente da decesso o malattie improvvise); questi ultimi sono nel complesso di durata insufficiente per verificare l’efficacia a lungo termine degli interventi (Vlaeyen E et al., 2015).
Gli studi mostrano un’ampia variabilità di setting di trattamento (Vlaeyen E et al., 2015) e carenze nel produrre una definizione univoca, standardizzata ed esplicita: di caduta, di disturbo neurocognitivo (Jensen J et al., 2003; Gonzàlez-Romàn L et al., 2016) e di cure usuali (Bunn F et al., 2014).
Valutazione dei disturbi cognitivi
I disturbi neurocognitivi sono certificati con test di misurazione dello stato neurocognitivo globale o scale di valutazione del comportamento o con la diagnosi clinica. I metodi per la loro individuazione e definizione possono influenzare la misurazione del livello di rischio di cadute: per esempio, i test di valutazione neurocognitiva non sono in grado da soli di accertare un rischio maggiore (Muir SW et al., 2012). Test come il MMSE senza l’utilizzo del giudizio clinico non riflettono in modo accurato lo stato neurocognitivo e funzionale di un soggetto: per esempio essi possono individuare un disturbo di qualsiasi tipo ma non diagnosticare una condizione di demenza (Shaw FE, 2007). Anche nei casi di diagnosi clinica di disturbo neurocognitivo non vi è distinzione fra le sue varie tipologie, a cui si associano eziologia, patologia di base, segni e sintomi, progressione di malattia e tassi di cadute differenti; ciò non consente di riconoscere più specificamente il beneficio degli interventi e impedisce la formulazione di conclusioni definitive (Vlaeyen E et al., 2015).
Considerazioni sulla popolazione bersaglio
La povertà di studi sulla prevenzione delle cadute in individui con disturbi neurocognitivi potrebbe essere un riflesso dei problemi metodologici ed etici derivanti dallo studio di questi soggetti, specie se istituzionalizzati, in quanto spesso con plurime comorbilità e grave compromissione funzionale (Shaw FE, 2007; Muir SW et al., 2012). Di particolare rilevanza sono i problemi legati alla randomizzazione e acquisizione del consenso informato, alla necessità di un approccio pluridisciplinare, del coinvolgimento del caregiver e/o di specifici gruppi di sostegno e all’incapacità dei partecipanti di rispettare le prescrizioni di interventi spesso complessi e poco flessibili per aderire alle diverse circostanze organizzative, logistiche e cliniche.
CONCLUSIONI
Sulla base dei risultati ottenuti dalle revisioni sistematiche incluse, attualmente permane incertezza sull’efficacia degli interventi di prevenzione delle cadute in soggetti con disturbi neurocognitivi e occorrono ulteriori studi per giungere a risultati più solidi, affidabili e generalizzabili. E’ probabile che, al peggiorare delle condizioni neurocognitive degli individui, per migliorare il tasso di successo in termini di riduzione delle cadute siano preferibili programmi di intervento multisfaccettati o multifattoriali rispetto a interventi singoli o multipli; tuttavia una maggiore complessità potrebbe essere di ostacolo a una aderenza e individualizzazione ottimali, a svantaggio dell’efficacia del trattamento.