Nell’85% delle Terapie Intensive (TI) vengono prescritti ai pazienti sedativi, con lo scopo di attenuare il dolore, l’ansia e l’agitazione derivata dalla ventilazione artificiale (Bambi et al., 2015). Una sedazione troppo alta potrebbe indicare una non corretta o superficiale gestione del dolore; una sedazione troppo bassa aumenta il rischio di auto-estubazione, problematiche cardiovascolari e danni fisici (Bambi et al., 2015). I livelli di sedazione dovrebbero variare a seconda delle esigenze di ogni paziente e del suo stato di malattia (Grap et al., 2012; Johansson et al., 2012).
Esistono raccomandazioni internazionali (Barr et al., 2013) che indicano necessario l’accertamento del dolore nel paziente critico incapace di comunicare e raccomandano il monitoraggio e la valutazione delle risposte comportamentali agli stimoli dolorosi. Si raccomanda inoltre l’adozione di strumenti che valutino parametri comportamentali e fisiologici come possibili indicatori di dolore nei pazienti ricoverati in TI, quali: espressione facciale, movimenti del corpo, tensione muscolare e compliance alla ventilazione meccanica (Pudas-Tahka et al., 2009).
Da una revisione sistematica (Pudas-Tahka et al., 2009) è stato evidenziato come solo due strumenti siano validi e affidabili nell’accertamento del dolore in TI: la Behavioral Pain Scale (BPS) (Payen et al., 2001) e la Critical-Care Pain Observation Tool (C-CPOT) (Gelinas et al., 2004, 2011; Gelinas and Arbour 2009). Le due scale sono validate in Italia già da alcuni anni (Stefani et al., 2011; Falbo et al., 2013).
Per quanto riguarda la gestione del dolore tra i pazienti intensivi, spesso si ricorre alla somministrazione di farmaci quali Paracetamolo e FANS, all’utilizzo dell’anestesia locoregionale, all’analgesia peridurale e all’infusione di oppioidi forti quali Remifentanil o Morfina ad alte dosi, spesso con diverse complicazioni sistemiche (depressione respiratoria, delirium, disturbi emodinamici) (Boom et al., 2012). Anche se la depressione respiratoria indotta da oppioidi può essere invertita rapidamente dall'antagonista del recettore oppioide Naloxone (30 minuti) (Boom et al., 2012), sono di recente sviluppo nuove tecniche di anestesia che vanno a trattare il dolore in modo più localizzato e con impatto più limitato a livello sistemico (Kamiya et al., 2018; Yalamuri et al., 2017; Tsai 2017). In quest’ottica, i blocchi dei fasci nervosi della parete addominale TAP block (transversus abdominis plane block) e pettorale PECS block (pectoralis and serratus plane blocks) hanno un grande campo di azione, tenuto conto della frequenza e dell’intensità dei dolori postoperatori (Dubost et al., 2012; Shaker et al., 2017; Yalamuri et al., 2017).
Il transversus abdominis plane, o TAP, corrisponde al piano situato tra i muscoli obliquo interno e trasverso. I blocchi riguardano i rami nervosi dei nervi intercostali T9-T12 e della prima radice lombare L1 (Tsai et al., 2017).
Il pectoralis and serratus plane, o PECS, corrisponde al piano del muscolo pettorale maggiore, il muscolo pettorale minore, il muscolo dentato anteriore e il muscolo succlavio. I blocchi riguardano per i muscoli pettorali maggiori e minori i nervi pettorali laterali e mediali, per il dentato anteriore il lungo nervo toracico (C5, C6 e C7) e per il succlavio il nervo del tronco superiore del plesso brachiale (C5 e C6) (Blanco, 2011). Queste iniezioni anestetiche interfasciali sono state sviluppate come alternative ai blocchi epidurali, paravertebrali, intercostali e intrapleurici del torace, e per tutta la chirurgia addominale.
Nell’ipotesi che gli strumenti di valutazione del dolore, così come le nuove tecniche di gestione siano ancora poco diffusi, con questo studio si vogliono esplorare i metodi di valutazione e gestione del dolore utilizzati nelle TI afferenti al Gruppo Italiano per la Valutazione degli Interventi in Terapia Intensiva (GiViTi).
Il nostro percorso
Nel periodo compreso tra Febbraio – Marzo 2018 è stata condotta una survey che ha coinvolto le TI appartenenti al GiViTi.
Per la raccolta dei dati è stato costruito un questionario ad hoc, volto ad esaminare valutazione e gestione del dolore in TI. Prima di procedere con la somministrazione del questionario è stata effettuata una validazione di contenuto ad opera di 2 Infermieri e 2 Medici di Terapia Intensiva esperti nella terapia del dolore.
Il questionario comprendeva:
- 3 domande riguardanti l’analisi di contesto (tipo di TI polivalente o specialistica; posti letto; pazienti ricoverati – adulti, pediatrici o neonati
- 4 domande riguardanti la valutazione del dolore
- 8 domande riguardanti la gestione del dolore.
In aggiunta è stato chiesto se negli ultimi 12 mesi all’interno della propria Azienda fossero stati organizzati corsi di aggiornamento specifici per il dolore rivolti a Medici e/o Infermieri.
Il questionario è stato creato tramite il software Survio e diffuso come un link allegato ad una lettera di presentazione, che rendeva esplicito lo scopo dell’indagine.
Risultati
Campione
Ha partecipato alla survey il 37,7% delle 515 T.I. contattate. I dati sono pervenuti da TI polivalenti (85.6%) e specialistiche (14.4%), con mediamente 8 posti letto per unità operativa. I pazienti assistiti presso le singole unità operative sono principalmente soggetti adulti: TI Pediatriche (3.6%), TI Adulti/Pediatriche (8.24%), TI adulti (88.14%).
Il 42% degli intervistati al momento della survey ha dichiarato che negli ultimi 12 mesi all’interno dell’Azienda sono stati organizzati corsi di aggiornamento per il dolore rivolti a Medici e Infermieri.
Valutazione del dolore
Tra le TI interpellate, il 75,3% delle TI ha affermato di utilizzare nel proprio servizio la Numerical Rating Scale (NRS) o la Verbal Numerical Scale (VNS) (Figura 1). Tra queste, l’87.7% ha dichiarato di effettuare un qualsiasi intervento antalgico quando NRS o VNS indicano uno score ≥ 4.
Tra le scale di valutazione specifiche per le aree critiche, la Behavioural Pain scale (BPS) è lo strumento più utilizzato (26.3%). Le scale BPS e C-CPOT, specifiche per le aree critiche, sono presenti nel 48.9% delle T.I rispondenti.
All’interno dell’88% delle TI il personale ha riferito di valutare il dolore chiedendo al paziente (quando sveglio e cosciente) o utilizzando uno strumento (scala BPS, CCPOT, PAINAD, altre) se il paziente è incapace di comunicare con lo staff medico-infermieristico.
Escludendo i pazienti curarizzati, profondamente sedati o tetraplegici (da qualsiasi causa), la maggioranza dei servizi (94.8%) ha affermato di valutare il dolore almeno una volta per turno.
Figura 1 – Scale di valutazione del dolore utilizzate nelle T.I. Italiane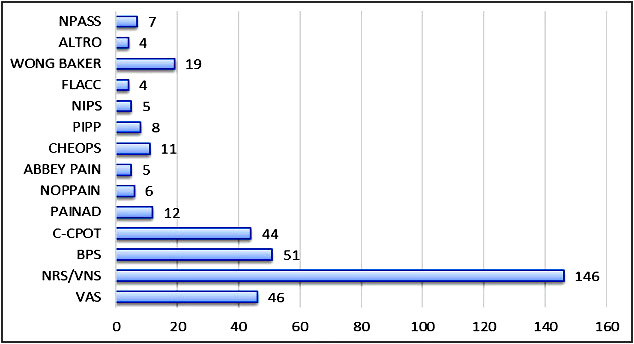
VAS = Visual Analogue Scale
NRS = Numerical Rating Scale
VNS = Verbal Numerical Scale
C-CPOT = critical care pain observation tool
BPS = Behavioural Pain Scale
PAINAD = Pain Assessment in Advanced Dementia
NOPPAIN = Non-Communicative Patient's Pain Assessment Instrument
ABBEY PAIN SCALE
CHEOPS = Children’s Hospital of Eastern Ontario Pain Scale
FLACC = Face Legs Activity Cry Consolability Scale
PIPP = Premature Infant Pain Profile
NIPS = Neonatal Infant Pain Scale
NPASS = Neonatal Pain Agitation and Sedation Scale
WONG BAKER.
Gestione del dolore
Il 79% dei servizi rispondenti ricorre a sedativi (Propofol, Midazolam, Dexmedetomidina) e oppioidi (Morfina, Remifentanil, Fentanyl) in infusione continua, per il mantenimento della sedo-analgesia durante le prime 72 ore di degenza in TI.
Considerando l’insieme delle TI intervistate, l’associazione sedo-analgesica più diffusa è Propofol-Morfina (81.4%).
Il farmaco maggiormente utilizzato per gestire il dolore nelle prime 24 ore di degenza è il Paracetamolo insieme al Ketoprofene (33%), solo il Paracetamolo (20.1%), solo il Ketoprofene (10.8%) (Figura 2).
Figura 2 – Farmaci maggiormente utilizzati per gestire il dolore nelle prime 24 ore di degenza in T.I.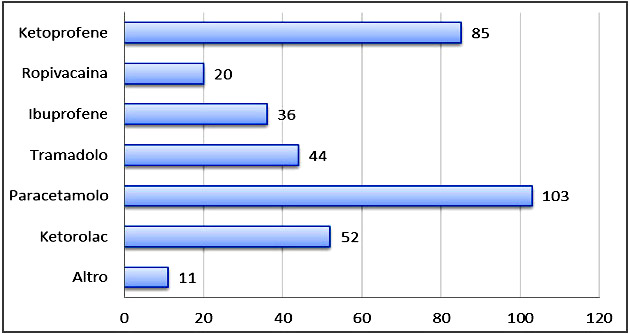
Il Paracetamolo 1 grammo ev a scopo analgesico viene somministrato in infusione in meno di 15 minuti (66.5%) o in base alla clinica del paziente (se paziente ipoteso o emodinamicamente instabile) (21.6%). La prescrizione di analgesici o antiinfiammatori ad orari fissi risulta la prescrizione più frequente (63%), piuttosto che la prescrizione al bisogno o sulla base di rilevazioni del dolore.
|
Tabella 1 – Sedativi e Oppioidi comunemente usati nelle T.I. italiane (prime 72 ore di degenza) come mantenimento della sedo-analgesia in infusione continua |
||||
|
Principio Attivo |
Meccanismo d’azione |
Dosaggio |
Proprietà farmacocinetiche |
Effetti avversi |
|
Propofol |
GABAA agonista. |
La velocità di somministrazione varia notevolmente tra pazienti, 4 e 12 mg/kg/h per mantenere un’adeguata anestesia. Pazienti pediatrici velocità di 9-15 mg/kg/h. |
Dopo infusione EV, l'emivita di eliminazione è variabile tra i 277 e i 403 minuti. La molecola viene escreta dall'organismo principalmente per via urinaria. Meno del 2% via gastroenterica. Metabolizzato da glucuronidazione epatica e idrossilazione. |
Vasodilatazione e inotropismo negativo, ipotensione e bradicardia (pressione sistolica e diastolica si riducono di circa il 30%). |
|
Midazolam |
GABAA agonista. |
Pazienti adulti: Dose di carico: 0,03 – 0,3mg/kg con incrementi di 1 – 2,5 mg. Dose di mantenimento: 0,03 – 0,2 mg/kg/h. |
Emivita da 3 a 11 ore. Il metabolita attivo si accumula con l’infusione prolungata; metabolizzato dall'ossidazione epatica, con escrezione renale del metabolita attivo. |
Stato confusionale, umore euforico,allucinazioni; bradicardia e ipotensione; nausea, vomito, costipazione, secchezza della bocca; dipendenza. |
|
Dexmedetomidina |
Agonista selettivo del recettore alfa-2. |
0.2 a 1.5 microgrammi/kg/hr. |
La dexmedetomidina per via endovenosa presenta una farmacocinetica lineare con un'emivita di distribuzione rapida di circa 6 minuti e un'emivita di eliminazione terminale di circa 2 ore. Viene metabolizzata dal fegato mediante glucuronidazione ed escreta nelle urine. |
Ipertensione transitoria, bradicardia, secchezza delle fauci, nausea. |
|
Morfina |
Agonista dei recettori μ-oppioidi (con effetti ulteriori da agonista sui recettori k-oppioidi e δ-oppioidi). |
Adulti: 15 mg somministrati per infusione lenta (dose urto): 0,8-80 mg/h (dose di mantenimento). |
Emivita da 3 a 7 ore. Insorgenza più lenta rispetto al fentanil con minore accumulo; metabolizzato dalla glicuronidazione epatica a morfina-6-glucuronide (10%) e morfina-3-glucuronide (90%), entrambi con escrezione renale. |
Nausea, costipazione, depressione respiratoria, rilascio di istamina e conseguente vasodilatazione e ipotensione. |
|
Remifentanil |
Agonista dei recettori μ-oppioidi (con effetti ulteriori da agonista sui recettori k-oppioidi). |
0,25-0,5 mcg/kg/min EV; eventuale bolo con 0,5-1 mcg/kg in risposta ad anestesia leggera o a episodi transitori di intenso stress chirurgico e procedurale. |
Emivita 3-4 min. Non si accumula con infusione prolungata; metabolizzato dalla esterasi plasmatica, quindi non influenzato dalla funzione degli organi. |
Nausea, costipazione, depressione respiratoria, bradicardia. |
|
Fentanyl |
Agonista dei recettori μ-oppioidi (con effetti ulteriori da agonista sui recettori k-oppioidi). |
0.7–10 μg/kg/hr infusione continua. |
Emivita variabile tra le 3 e le 12 ore. Viene metabolizzato principalmente a livello epatico. Eliminazione avviene prevalentemente per via urinaria, sotto forma di metaboliti e solo un 10% circa come farmaco immodificato. |
Nausea, costipazione, depressione respiratoria, rigidità muscolo-scheletrica con alte dosi di bolo. |
Relativamente alla gestione dei traumi toracici, la tecnica PECS block è stata utilizzata negli ultimi 3 mesi in 16 TI (8.2%) per il trattamento di almeno un paziente, mentre il 78.1% dei servizi gestisce i traumi o politraumi con limitazioni nella mobilizzazione, con oppiodi forti in infusione continua ev. (Morfina, Remifentanyl, Fentanyl), più aggiunta di adiuvanti (Paracetamolo o FANS).
Relativamente alla gestione del dolore addominale, la tecnica TAP block è stata usata negli ultimi 3 mesi dal 7.2% delle unità intervistate per il trattamento di almeno un paziente. La gestione avviene principalmente con oppiodi forti in infusione continua ev (Morfina, Remifentanyl, Fentanyl), e Paracetamolo (73.2%).
Discussione
Dalla survey è emerso come gli strumenti di valutazione specifica del dolore per le TI siano diffusi nel 49% delle stesse. Le ultime linee guida per le aree critiche sottolineano l’importanza dell’utilizzo di strumenti validati (Barr et al., 2013). I parametri vitali non sono ottimi indicatori della presenza o assenza di dolore; tuttavia la loro variazione può essere utilizzata come dato base per la ricerca di eventuali cause e fonti di dolore (Barr et al., 2013).
Nonostante gli oppioidi non siano sempre esenti da effetti avversi, le informazioni pervenute dall’indagine evidenziano come la maggioranza dei servizi di area critica ricorra all’infusione costante di oppiodi e sedativi per la gestione del dolore, almeno per le prime 72 ore della degenza (Tabella 1).
Nell’ambito di una gestione multimodale, l’utilizzo dell’anestesia locoregionale (ALR) è raccomandata tutte le volte possibili, a complemento delle tecniche di analgesia classica (Dubost et al., 2012). In generale la combinazione di FANS e Paracetamolo, spesso riscontrate nelle varie realtà operative, fornisce una maggiore analgesia rispetto al solo Paracetamolo per il trattamento del dolore acuto nei traumi e dopo chirurgia ortopedica (Ong et al., 2010).
Dai risultati della survey le tecniche PECS e TAP block risultano ancora poco diffuse sul territorio nazionale.
E’ importante sottolineare che tra i pazienti sottoposti a chirurgia toracica, la PECS block combinata con l'anestesia generale riduce il fabbisogno di sedazione da Propofol (Kamiya et al., 2018). L’utilizzo di questa tecnica può fornire un importante opzione non oppioide per la gestione del dolore, in quanto i pazienti vengono svezzati rapidamente dall'ossigeno supplementare grazie al miglioramento dell'analgesia (Yalamuri et al., 2017). Tuttavia non sempre si nota una riduzione di oppioidi forti come il Remifentanil, a causa dell'incapacità dei blocchi nervosi di raggiungere l'area mammaria interna (Kamiya et al., 2018).
Allo stesso tempo, i pazienti di chirurgia addominale vengono trattati con analgesia peridurale o con oppioidi forti, quali Morfina, con diverse complicazioni sistemiche (es. insufficienza respiratoria, delirium, disturbi emodinamici). La tecnica TAP block può essere una valida alternativa.
L’interesse clinico di questa tecnica di anestesia è stata validata da studi clinici, dopo gastrectomia (Ari et al., 2107), colectomia, isterectomia e cesareo (Salaria et al., 2017). Numerosi altri studi e casi clinici suggeriscono l’interesse di questo blocco in tutta la chirurgia addominale (Shacker et al., 2017). L'uso del TAP block è associato a un minor uso parenterale di Morfina equivalente e ad una diminuita incidenza di ipotensione nel primo periodo post-operatorio rispetto all’analgesia epidurale toracica (TEA) (Shacker et al., 2017).
Limiti
Lo studio presenta vari limiti. Lo strumento di indagine (un questionario costruito ad hoc) ha subito un processo di validazione di contenuto da parte di un team di esperti, ma la validazione ha riguardato solo item, istruzioni, codifica delle risposte e coerenza delle domande con il costrutto target e nessun indice di concordanza è stato scelto o fissato.
Per il raggiungimento delle informazioni è stato scelto a priori un campione di convenienza (TI iscritte all’associazione GiViTi) rapidamente accessibile, che però non rappresenta la totalità delle TI italiane.
Delle 515 unità operative contattate, il 62.3% non ha preso parte all’indagine. Questo espone i nostri risultati ad attrition bias.
Conclusioni
Lo studio intendeva esplorare un campione rappresentativo delle TI italiane al fine di evidenziarne strumenti e metodi di valutazione e gestione del dolore. Il risultato ci porta ad evidenziare come le scale di valutazione specifiche per l’area critica (BPS e C-CPOT) siano diffuse nel 50% circa dei rispondenti, mentre le tecniche di gestione più recenti quali la TAP o la PECS block sono per lo più assenti. Il Paracetamolo è un farmaco comune, con una prescrizione diffusa, e non vi è dubbio che continuerà ad essere un analgesico utile sia in fase acuta che cronica, da solo o in combinazione con FANS e oppioidi per la sua notevole sicurezza e interazioni minime con altri farmaci (Graham et al., 2013). L’epatotossicità Paracetamolo-correlata, a dosi eccessive, è un chiaro problema, ma le prove che dimostrano la certezza della tossicità per dosi di 4 g/die sono discutibili (Graham et al., 2013).
Nel panorama nazionale emerge una discreta omogeneità nel modo di valutare e gestire il dolore. Ricerche future dovranno valutare l’impatto di strumenti di valutazione specifici per i contesti di area critica (scale BPS e C-CPOT) sul dolore e sulla sua relativa gestione, valutando l’utilità di training formativi per il personale medico ed infermieristico. Sono in aggiunta auspicabili revisioni sistematiche e meta-analisi riguardo l’efficacia della PECS e TAP block nella gestione del dolore postoperatorio.