L’Angioedema Ereditario (HAE) è una patologia genetica rara, dovuta ad una mutazione del gene che codifica per il C1 inibitore (C1-INH) localizzato sul cromosoma 11 (11q12-q13.1) (Carugati et al., 2001). Si trasmette con carattere autosomico dominante a penetranza completa (Agostoni et al., 1992).
L’Angioedema Ereditario è causato dal difetto genetico della proteina inibitrice del sistema complementare. Il sistema complementare è implicato nell’immunità innata e regola l’omeostasi vascolare, la difesa dai patogeni, l’eliminazione dei detriti cellulari e la chiarificazione degli immunocomplessi (Caliezi et al., 2000). Il difetto di C1 inibitore provoca l’attivazione incontrollata di tale sistema, con l’aumentata produzione di Bradichinina e la comparsa di edemi localizzati nei tessuti sottocutanei e sottomucosi di differenti distretti corporei (Figura 1). Le manifestazioni gastroenteriche possono essere tanto gravi da simulare un quadro obiettivo di addome acuto. L’evento più temuto è rappresentato dall’edema della laringe, il quale può provocare morte per asfissia.
Figura 1 – Sedi di Angioedema nei vari organi e distretti (Bork et al., 2006)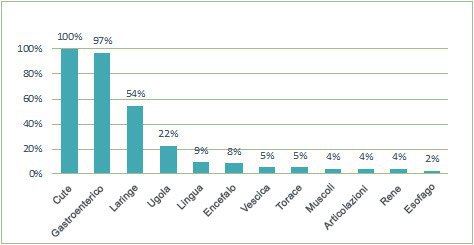
L’Angioedema Ereditario viene classificato a seconda della gravità dei sintomi in:
- Lieve – non interferisce con le attività del paziente;
- Moderato – alcune attività sono di difficile esecuzione, ma il paziente provvede autonomamente;
- Moderato-Severo – alcune attività sono di difficile esecuzione ed il paziente necessita di un supporto terapeutico per modificare la sua condizione, oppure la localizzazione della manifestazione comporta il rischio di evolvere in Edema laringeo (edema periorale o del collo);
- Severo – impossibilità di dedicarsi a qualunque attività, il paziente necessita di supporto terapeutico (localizzazione oro-faringea).
Fattori che possono facilitarne l’insorgenza sono: traumi, interventi chirurgici, infezioni, cambiamenti ormonali nelle donne (es. ciclo mestruale, gravidanza, parto), farmaci contenenti estrogeni ed alcuni farmaci per l’ipertensione, quali Ace-inibitori. La sintomatologia può durare da qualche ora a qualche giorno, può essere autolimitante o migrare verso altri distretti corporei.
Come tutte le malattie rare, anche l’Angioedema Ereditario è difficile da diagnosticare se non prontamente valutato in un centro specializzato nella diagnosi e cura. Nelle malattie rare si stima che mediamente occorrano dai 3 ai 5 anni per giungere alla diagnosi; nel caso specifico dell’HAE la diagnosi può arrivare anche dopo 15 anni dall’esordio dei sintomi (Banerji et al., 2015).
In Italia si registra una prevalenza di 1:66.000 (Zanichelli et al., 2015). L’età di esordio degli episodi acuti è variabile e colpisce sia uomini che donne; nella maggior parte dei casi si manifesta entro la seconda decade di vita. La frequenza e la gravità degli attacchi è variabile anche tra gli individui di uno stesso nucleo familiare che condividono la medesima mutazione puntiforme.
Per la diagnosi di HAE devono essere presenti almeno un criterio clinico ed un criterio di laboratorio (Tabella 1).
|
Tabella 1 – Criteri diagnostici per l’HAE (Bowen et al., 2010) |
|
|
Criteri clinici |
Angioedema sottocutaneo, non pruriginoso, non eritematoso, autolimitante, solitamente ricorrente e di lunga durata (più di 12 ore), senza orticaria, talvolta preceduto da un eritema serpiginoso. |
|
Dolori addominali ricorrenti (spesso con vomito e/o senza diarrea), senza causa organica, a risoluzione spontanea in 12-72 ore. |
|
|
Edemi laringei ricorrenti. |
|
|
Storia familiare conclamata di Angioedema da carenza del C1 inibitore. |
|
|
Criteri di laboratorio |
Livelli antigenici di C1 inibitore <50% del normale in 2 determinazioni separate e dopo il primo anno di vita. |
|
Livelli di attività funzionante di C1 inibitore <50% del normale in 2 determinazioni separate dopo il primo anno di vita. |
|
|
Mutazione del gene di C1 inibitore che altera la sintesi e/o la funzionalità della proteina. |
|
Terapia
La terapia dell’attacco acuto di Angioedema dipende dal distretto coinvolto e dalla gravità dei sintomi. Nei pazienti con edema laringeo, manifestazioni gastroenteriche e/o cutanee particolarmente severe, la terapia di primo livello comprende uno dei seguenti farmaci:
- Inibitore della Callicreina somministrato per via sottocutanea;
- C1 inibitore umano per via endovenosa;
- Antagonista del recettore B2 della Bradichinina per via sottocutanea.
Questi ultimi due farmaci rappresentano la strategia di trattamento autorizzata per la Self-Administration (Bork et al., 2012). Nei dipartimenti d’emergenza, in caso di mancata disponibilità di farmaci specifici, è possibile somministrare, da parte del personale sanitario, plasma fresco congelato alla dose iniziale di 2 unità (Pekdemir et al., 2007).
Home Therapy
Essendo una patologia rara, l’HAE risulta essere poco conosciuto in ambiente sanitario. Non di rado, in regime di emergenza/urgenza, la patologia viene trattata come reazione anafilattica mediante la somministrazione di cortisonici ed antistaminici a cui l’HAE non risponde, con conseguente peggioramento del quadro clinico. Gli attacchi acuti dell’HAE, come ricordiamo, sono modulati dalla Bradichinina e non dall’Istamina. È, pertanto, da tali problematiche che nasce il programma di Home Therapy.
Per Home Therapy e Self-Administration si intende il trattamento terapeutico, conferito in un ambiente non sanitario, da parte del paziente o del caregiver addestrato, al di fuori di una struttura sanitaria (Cicardi et al., 2013). Secondo recenti raccomandazioni, tutti i pazienti dovrebbero avere accesso al farmaco C1-INH plasmatico ricombinante per il trattamento degli attacchi acuti gravi (Cicardi et al., 2012). Con la diffusione di farmaci presso il domicilio, pertanto, nasce l’esigenza di educare il paziente ed il caregiver nella tecnica di auto-somministrazione della terapia o Self-Administration.
La Self-Administration permette di risolvere gli eventi acuti in modo rapido e sicuro, conferisce ai pazienti maggiore fiducia ed autostima, riduce la morbilità, l’assenteismo, i costi e gli oneri derivanti dalla patologia, oltre che la potenziale mortalità da eventi gravi, garantendo un eccellente profilo di sicurezza (Bork et al., 2005). In caso di edema laringeo i pazienti dovranno recarsi in egual modo presso il Pronto Soccorso più vicino.
L’Home Therapy non presenta limiti d’età per l’apprendimento; tuttavia i bambini necessitano della presenza di un adulto disposto ad intraprendere il percorso di formazione, in quanto diverrà responsabile dell’autocura (Abdel-Karim et al., 2014). Uno studio condotto a Francoforte nel 2010, che ha incluso 15 pazienti pediatrici (età media 14 anni), ha ottenuto risultati di sicurezza ed efficacia paragonabili a quelli dell’intera popolazione: drastica riduzione del tempo tra insorgenza del sintomo e trattamento (da 67,5 minuti a 15 minuti) e riduzione del numero medio annuo di giorni in ospedale (da 3.8 a 0.11) (Abdel-Karim et al., 2014). Il programma di Home Therapy è raccomandato anche nelle donne in gravidanza ed allattamento (Martinez-Saguer et al., 2010).
Ulteriore testimonianza del successo del programma di Home Therapy rispetto al trattamento convenzionale si ha da uno studio italiano, dove sono stati rilevati riduzione del numero di ospedalizzazioni (da 16,8 a 2,1), riduzione dei giorni di assenza da lavoro/scuola (da 20,3 a 7,1) e diminuzione dei costi medici (risparmio di 11,3%) (Petraroli et al., 2015).
Nell’ospedale universitario di Francoforte, dove la terapia C1-INH è disponibile da molti anni, il 49% dei pazienti è in grado di autosomministrarsi il farmaco (Dispenza et al., 2012). Uno studio danese ha messo inoltre in evidenza che il 39% dei pazienti da loro seguiti stesse già praticando l’autoterapia per il trattamento degli eventi acuti (Rusicke et al., 2006).
Nonostante i numerosi studi condotti, l’Home Therapy è vista tuttora con riluttanza e preoccupazione da parte del personale sanitario (Maurer et al., 2013).
Self-Administration e responsabilità infermieristiche
La Self-Administration dei farmaci rappresenta la pratica mediante la quale il paziente può trattare gli attacchi al loro esordio in modo autonomo ed indipendente, senza necessità di recarsi presso una struttura sanitaria. Può realizzarsi a condizione che il paziente si assuma la responsabilità dell’assunzione dei farmaci prescritti. A seconda dei gradi di automedicazione, vi sono diversi livelli di responsabilità, che dovranno essere chiaramente documentati (Leitch et al., 2017). La partecipazione al programma di Home Therapy deve essere basata su criteri di valutazione dell’idoneità, sicurezza del sistema, scelta informata e consenso da parte del paziente.
È possibile identificare 3 fasi del processo:
- Fase 1 – Il farmaco verrà dispensato al paziente da personale autorizzato nel momento più appropriato. Il processo di Self-Administration è svolto sotto stretta supervisione del personale sanitario;
- Fase 2 – Il paziente è abilitato nel detenere, presso il proprio domicilio, una limitata offerta di farmaci; il livello di fornitura è determinato da fattori che derivano dalla valutazione e decisione del team multidisciplinare. Occorre controllare quotidianamente, da parte del personale, che il paziente agisca in sicurezza, ad esempio indicando un luogo idoneo da allestire per la somministrazione del farmaco ed identificando un posto per la conservazione dello stesso;
- Fase 3 – Il paziente diventa completamente responsabile dell’autocura, identificando il momento appropriato, oltre che della corretta conservazione dei farmaci in un posto sicuro designato.
Affinché il paziente possa intraprendere il percorso formativo, l’infermiere dovrà valutare dei criteri di inclusione standardizzati (Tabella 2); tali criteri sono stati messi a punto nel 2005, mediante linee guida e dichiarazioni di consenso (Gompels et al., 2005), e sottoposti ad ulteriore revisione nel 2013 (Cicardi et al., 2013).
|
Tabella 2 – Criteri per l’accesso al programma di Home Therapy (Gompels et al., 2005) |
|
Carenza di C1-INH accertata. |
|
La conformità e l’uso della profilassi farmacologica da parte del paziente dovrebbero essere ottimali. |
|
Al fine di mantenere le capacità di infusione richieste, il paziente dovrebbe normalmente richiedere l’infusione di C1-INH almeno ogni 3 mesi. |
|
Il paziente deve essere motivato nel rispettare il programma di Home Therapy e tutte le sue implicazioni, ed essere disposto ad esserne responsabile. Il consenso deve essere scritto e deve essere ottenuto prima che il programma venga avviato. |
|
Il paziente deve essere informato riguardo al rischio di infezioni trasmissibili. Il paziente deve dimostrare di aver compreso le informazioni e fornire il consenso informato scritto per l’adesione. |
|
Il paziente deve avere un partner desideroso di partecipare al programma di Home Therapy, il quale sarà presente quando è richiesta la terapia. |
|
La conferma scritta per l’adesione al programma di Home Therapy deve essere concordata con il medico di base del paziente, includendo il supporto ed il percorso concordato in caso di emergenza. |
|
Il paziente deve avere accesso ad un telefono quando si somministra la terapia. |
|
Il paziente deve possedere un buon accesso venoso. |
|
Il paziente deve accettare di richiedere un’ambulanza nel caso di insuccesso dell’autosomministrazione del farmaco. |
|
Nella maggior parte delle circostanze l’Home Therapy non è impiegata nei bambini. |
Esistono documenti di consenso che standardizzano le tematiche da trattare durante la formazione del paziente (Tabella 3) e che hanno ottenuto il riconoscimento internazionale nel 2009 (Longhurst et al., 2010).
|
Tabella 3 – Programma di formazione per Home Therapy (Gompels et al., 2005) |
|
Uso appropriato del concentrato del farmaco. |
|
Lavaggio delle mani e tecnica asettica. |
|
Fornitura e stoccaggio di concentrati e presidi. |
|
Preparazione per la somministrazione del concentrato. |
|
Procedura di controllo del prodotto, in termini di dosaggio e data di scadenza. |
|
Dimostrazione della tecnica corretta per la ricostituzione della soluzione. |
|
Venipuntura mediante Ago-Butterfly. |
|
Prelievo di sangue pre-iniezione/infusione. |
|
Somministrazione dell’iniezione/gestione dell’infusione. |
|
Gestione delle reazioni avverse. |
|
Gestione dell’Adrenalina/Epinefrina iniettabile (per il trattamento dell’anafilassi dell’infusione). |
|
Smaltimento dei presidi. |
|
Documentazione e Registrazione precisa del numero del lotto. |
|
Documenti di formazione e competenze dell’individuo. |
|
Ricevere e monitorare i protocolli di infusione ed altri documenti pertinenti per qualsiasi difficoltà. |
|
Esaminare eventuali reazioni avverse e prendere le misure appropriate. |
|
Informare l’infermiere/consulente specialista immunologo su tutte le questioni relative la cura ed il trattamento. |
|
Compliance alle visite cliniche. |
|
Eseguire rivalutazioni annuali delle competenze dell’individuo per la gestione dell’iniezione/infusione. |
|
Comunicazione tra il paziente, il medico di base, l’immunologo di riferimento ed altri operatori sanitari garanti assistenza. |
Designare un percorso terapeutico-assistenziale personalizzato permette al paziente di affrontare con consapevolezza tutti gli aspetti riguardanti la propria patologia ed il trattamento degli eventi acuti, e di ampliare ed approfondire le competenze infermieristiche nei confronti di patologie ereditarie rare.
L’infermiere:
- fornisce le informazioni riguardanti la pratica di Home Therapy e Self-Administration, informa il paziente ed il caregiver su eventuali rischi e responsabilità che tale scelta comporta. Il team multidisciplinare definirà le priorità e le competenze che la persona dovrà padroneggiare, identificando le differenti azioni che caratterizzano determinati compiti. Occorre in tale processo tenere presente la complessità e l’inusualità del percorso per il paziente, oltre che lo stato d’animo in cui si trova (Benini, 2010). Il paziente deve essere guidato nel maturare competenze in termini di: comprensione di sé stesso, della malattia e del relativo trattamento, capacità di auto-sorveglianza, autocura e adattamento della terapia al proprio stile di vita;
- valuta i criteri di inclusione definiti da documenti di consenso standardizzati per l’adesione del paziente al programma formativo di Self-Administration;
- educa ed addestra il paziente ed il caregiver. Il percorso formativo si compone di due sessioni (Petraroli et al., 2015). Durante la sessione teorica, l’infermiere trasferirà con termini semplici nozioni riguardanti la patologia, la gestione degli attacchi acuti, l’organizzazione delle proprie attività quotidiane in rapporto al proprio stato di salute, lo stile di vita da adottare e l’individualizzazione precoce delle complicanze; verranno formulati degli schemi con passi sequenziali da compiere in caso di edemi gravi ed eventuali complicanze associate alla somministrazione del farmaco. Durante la sessione pratica, l’infermiere illustrerà mediante l’ausilio di un braccio simulatore le tecniche di infusione endovenosa ed iniezione sottocutanea. Al domicilio del paziente dovrà essere individuato un luogo sicuro da allestire per l’autosomministrazione e per la conservazione del farmaco;
- seleziona l’accesso vascolare più idoneo per il paziente. La fase più delicata del processo di formazione è rappresentata dall’indicare al paziente ed al caregiver le tecniche di infusione endovenosa ed iniezione sottocutanea. Nel caso della somministrazione endovenosa, per ridurre i danni da venipuntura o eventuale stravaso è consigliato un ago-butterfly da 28 Gauge (Longhurst et al., 2010). Ingenti difficoltà si riscontrano quando il patrimonio vascolare del paziente risulta essere esiguo; a tal proposito, è stata aperta la possibilità ai pazienti affetti da HAE di adoperare un dispositivo di accesso vascolare totalmente impiantabile (Port-a-cath) (Riedl et al., 2017). Si può determinare in in tal modo una riduzione delle complicanze derivanti dalla difficoltà di reperimento dell’accesso vascolare, stravaso o mancata somministrazione del farmaco. Occorre ricordare, tuttavia, che il dispositivo di accesso vascolare totalmente impiantabile richiede un’attenta gestione, al fine di ridurre problematiche in termini di occlusione, trombosi ed infezioni;
- assiste, supervisiona ed incoraggia il paziente ed il caregiver durante tutto il percorso formativo per il raggiungimento dell’autonomia;
- valuta le capacità acquisite e gli obiettivi raggiunti dal paziente e dal caregiver; qualora non siano idonei o pronti, ciò dovrà essere documentato. Il personale infermieristico monitorerà eventuali difficoltà nella somministrazione del farmaco; talora, può rendersi necessario per i pazienti tornare alle fasi precedenti o, addirittura essere esclusi dal regime di Self-Administration.
Complessivamente, la velocità di apprendimento da parte dei pazienti risulta essere sorprendente, spesso sono necessarie solo alcune ore (Symons et al., 2013). L’aggiornamento delle conoscenze del paziente e del caregiver è previsto ogni 12 mesi (Longhurst et al., 2010). Poiché i pazienti possono dimenticare parti della loro formazione, la presenza di dépliant, opuscoli e fogli di controllo può contribuire nel garantire che tutti i kit siano preparati in modo appropriato e che tutto venga svolto nella sequenza corretta.
Barriere per l’autosomministrazione
Uno studio condotto negli Stati Uniti ha tentato di valutare le esperienze degli infermieri e le eventuali barriere riscontrate: è emerso che gli infermieri ritengono necessario un percorso di apprendimento più lungo. Pochi pazienti hanno rifiutato di intraprendere l’autosomministrazione in seguito all’insegnamento iniziale, ed i motivi principali includono la paura dell’iniezione e dell’infezione, la mancanza di competenze, l’interferenza nelle attività quotidiane e le restrizioni finanziarie (Tuong et al., 2014). In alcuni contesti la Self-Administration è accettata con riluttanza, da parte del personale sanitario, riconducibile, perlopiù, alla preoccupazione di un eventuale uso inappropriato del farmaco da parte del paziente.
Conclusioni
La pratica di Self-Administration non si sostituisce in alcun modo alle competenze mediche ed infermieristiche. Home Therapy e Self-Administration nascono, esclusivamente, dalla volontà di migliorare la qualità di vita dei pazienti, insegnando loro come convivere con la propria patologia, come limitare le complicanze e come intervenire nell’eventualità di manifestazioni gravi. Pertanto, anche in seguito al raggiungimento di autonomia, i pazienti avranno, sempre, un saldo punto di riferimento nel personale infermieristico e medico del Centro di Diagnosi e Cura competente.
L’Home Therapy, con adeguati criteri di sicurezza, permette di ridurre i costi sanitari, migliorare qualitativamente la vita dei pazienti ed ottenere una rapida risoluzione degli attacchi acuti derivanti dalla patologia. La prospettiva futura è di poter estendere tale alternativa terapeutica ad altre patologie ereditarie cronico-invalidanti, come già accade per i pazienti affetti da Angioedema Ereditario ed Emofilia.






